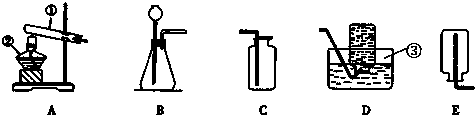题目内容
实验室对氯酸钾和二氧化锰混合制取氧气后的剩余固体进行了如下实验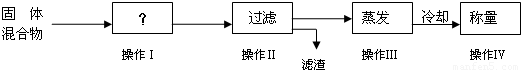
①写出操作Ⅰ的名称______;
②操作Ⅳ称量所得的固体为1.49g(不计每步操作损耗),请问该实验中氯酸钾和二氧化锰混合加热,产生了多少molO2?(根据化学方程式列式计算)
【答案】分析:要将二氧化锰从混合物中分离出来,首先将固体溶解再进行过滤;根据操作过程可知:操作Ⅳ所得固体为氯化钾,根据氯化钾的质量并结合方程式可减少出生成氧气的物质的量.
解答:解:(1)要将二氧化锰从混合物中分离出来,首先将固体溶解再进行过滤;
故答案为:溶解;
(2)氯化钾的物质的量为: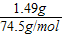 =0.02mol
=0.02mol
设生成O2x mol.
2KClO3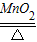 3O2↑+2KCl
3O2↑+2KCl
3 2
x 0.02mol
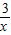 =
=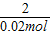
x=0.03mol
答:生成O20.03mol.
点评:本题考查了学生获取信息,及利用方程式规范答题的能力,要细心分析,仔细解答.
解答:解:(1)要将二氧化锰从混合物中分离出来,首先将固体溶解再进行过滤;
故答案为:溶解;
(2)氯化钾的物质的量为:
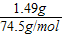 =0.02mol
=0.02mol 设生成O2x mol.
2KClO3
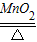 3O2↑+2KCl
3O2↑+2KCl 3 2
x 0.02mol
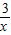 =
=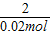
x=0.03mol
答:生成O20.03mol.
点评:本题考查了学生获取信息,及利用方程式规范答题的能力,要细心分析,仔细解答.

练习册系列答案
相关题目
(1)实验室中常用氯酸钾和二氧化锰加热制氧气、锌粒与稀硫酸反应制氢气、石灰石与稀盐酸制二氧化碳气体.

写出标号仪器的名称① ②
请结合所给药品选择适当的气体发生和收集装置填入下表:(填字母)
(2)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题.某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量.
①仪器B的作用是 .
②仪器E中的现象是 .
③若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重a g,则Wg该塑料试样中含氢元素的质量为 g(计算结果可为分数形式)
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果 (填“偏小”、“偏大”、“无影响”中之一).

写出标号仪器的名称①
请结合所给药品选择适当的气体发生和收集装置填入下表:(填字母)
| 气体 | 发生装置 | 收集装置 |
| O2 | ||
| H2 | ||
| CO2 |

①仪器B的作用是
②仪器E中的现象是
③若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重a g,则Wg该塑料试样中含氢元素的质量为
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果
某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究.请你参与探究并回答下列问题.

(1)完成下表:
如图:
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是 原因是: .
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是 (填写选项序号).
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当 停止加热.
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为 .请在装有所配制溶液的试剂瓶(如图)标签上标明相应信息.
④过滤、溶解、蒸发时都需用到的仪器是 (填序号);
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是 .

(1)完成下表:
| 气 体 | 药 品 | 装置组合 | 反应的化学方程式 |
| 氧 气 | 氯酸钾和二氧化锰 | ||
| 氢 气 | 稀盐酸与锌粒 | A、C | |
| 二氧化碳(干燥) | 大理石和稀盐酸 |
(2)以下是菲菲同学制取二氧化碳主要操作过程的示意图

她操作中的错误是
(3)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),
①通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
a、烘干b、溶解c、过滤d、洗涤
②把滤液蒸发结晶可得到氯化钾晶体,在蒸发过程中,当
③如果用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,则需要氯化钾的质量为

④过滤、溶解、蒸发时都需用到的仪器是
A、酒精灯B、烧杯C、玻璃棒D、漏斗E、量筒
(4)小明用6.5 g含有铜、铝、铁或镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌块中一定含有的金属杂质是