题目内容
在日常生活中,我们发现切过咸菜的刀更容易生锈,而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
【步骤一】未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要验证紫红色固体中是否含有氧化铜,可用________(填一试剂)加以检验。
【步骤二】未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是__________________________。
【步骤三】打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将下表“影响因素”选项前恰当的字母序号填入指定位置。
| 实验操作 | 实验现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 现象二:粗砂纸打磨的片刻内现象不明显。 | 现象一与现象二对比,说明: ①____________ |
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象三与现象一对比,说明:②________;现象四与现象三对比,说明:③__________ |
★影响因素:
A.打磨时用力程度及均匀程度不同 B.选用砂纸颗粒粗细程度不同
C.由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是______________________________。
(5)请仔细观察下图。
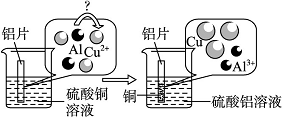
试从微观粒子变化的角度分析该反应的实质:_______________________________。
答案:(1)稀盐酸或稀硫酸
(2)氯离子对金属及其氧化物的结构具有较强的破坏作用(或氯离子促使反应进行)
(3)①A ②B ③AC
(4)证 实氧化膜对反应的影响
实氧化膜对反应的影响
(5)在溶液中,铝比铜活泼,每2个铝原子失去6个电子,变成2个铝离子;每3个铜离子得到6个电子,变成3个铜原子
解析:(1)金属氧化物能够与酸发生反应;
(2)未打磨的铝片表面有一层保护膜,当加入CuCl2溶液时迅速反应,说明了Cl-对氧化物有较强的破坏性等;
(3)仔细比较现象一和二知:粗砂纸打磨的均匀程度不一样,带来的结果就不一样;而现象三和一分别选用了细砂纸和粗砂纸;现象四与三都选用了细砂纸但打磨的时间不一样,用力程度也不一样;
(4)以上几个实验都是为了不同程度地破坏氧化膜;
(5)由图示知:在溶液中Al的活动性比Cu强。

 如图是某些国家的人均水量和世界人均水量柱状图.
如图是某些国家的人均水量和世界人均水量柱状图. 于水 (填“放热”或“吸热“)。生活用水在净化过程中常用 吸附色素和异味,一般可以通过 的方法降低水的硬度。
于水 (填“放热”或“吸热“)。生活用水在净化过程中常用 吸附色素和异味,一般可以通过 的方法降低水的硬度。 一点有效措施有
一点有效措施有  于水 (填“放热”或“吸热“)。生活用水在净化过程中常用 吸附色素和异味,一般可以通过 的方法降低水的硬度。
于水 (填“放热”或“吸热“)。生活用水在净化过程中常用 吸附色素和异味,一般可以通过 的方法降低水的硬度。 一点有效措施有
一点有效措施有