题目内容
26、某化学实验小组为测定生石膏的组成(CaSO4?xH2O),即测x的值,做了如下实验,将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量,随着实验次数的增加,加热的时间不断延长.它们的实验数据理如下:
利用数据可绘制成以下图象:

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
| 实验顺序 (按序延长加热时间) |
固体质量/g | |
| 加热前 | 后 | |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
| 8 | 3.44 | 2.72 |

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
分析:根据题意可知加热前和加热后质量的减少量就是生成水的质量,由实验数据知3.44g CaSO4?xH2O完全分解得到无水CaSO42.72g,可知生成水的质量为:3.44g-2.72g=0.72g,由水的质量和硫酸钙的质量可推算出生石膏的化学式,再根据A-B段时石膏的质量为2.90g,其中CaSO42.72g,H2O0.18g,所以图象中产生AB段的原因是石膏的质量为2.90g,其中CaSO42.72g,H2O0.18g.此时其化学式可表示为2CaSO4?H2O.
解答:(1)解:石膏加热分解减少的质量就是水的质量,由实验数据知3.44g CaSO4?xH2O完全分解得到无水CaSO42.72g,则:
CaSO4?xH2O═CaSO4+xH2O
136 18x
2.72 0.72
即136:2.72=18x:0.72 解得x=2 所以石膏的化学式为CaSO4?2H2O.
(2)由实验数据知在A-B段时石膏的质量为2.90g,其中CaSO42.72g,H2O0.18g.此时其化学式可表示为2CaSO4?H2O.
故答案为:
(1)CaSO4?2H2O;
(2)2CaSO4?H2O.
CaSO4?xH2O═CaSO4+xH2O
136 18x
2.72 0.72
即136:2.72=18x:0.72 解得x=2 所以石膏的化学式为CaSO4?2H2O.
(2)由实验数据知在A-B段时石膏的质量为2.90g,其中CaSO42.72g,H2O0.18g.此时其化学式可表示为2CaSO4?H2O.
故答案为:
(1)CaSO4?2H2O;
(2)2CaSO4?H2O.
点评:解答本题的主要的原因是反应前后质量的减少量就是生成水的质量,再根据实际情况进行进一步分析.

练习册系列答案
相关题目
某化学实验小组为测定生石膏的组成,即测x的值,做了如下实验,将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量,随着实验次数的增加,加热的时间不断延长.它们的实验数据理如下:
利用数据可绘制成以下图象:
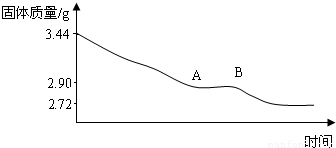
(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
| 实验顺序 (按序延长加热时间) | 固体质量/g | |
| 加热前 | 加热后 | |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
| 8 | 3.44 | 2.72 |

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
某化学实验小组为测定生石膏的组成,即测x的值,做了如下实验,将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量,随着实验次数的增加,加热的时间不断延长.它们的实验数据理如下:
利用数据可绘制成以下图象:

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
| 实验顺序 (按序延长加热时间) | 固体质量/g | |
| 加热前 | 加热后 | |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
| 8 | 3.44 | 2.72 |

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
某化学实验小组为测定生石膏的组成,即测x的值,做了如下实验,将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量,随着实验次数的增加,加热的时间不断延长.它们的实验数据理如下:
利用数据可绘制成以下图象:
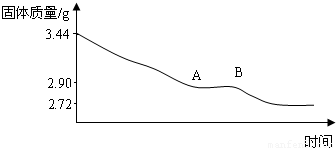
(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
| 实验顺序 (按序延长加热时间) | 固体质量/g | |
| 加热前 | 加热后 | |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
| 8 | 3.44 | 2.72 |

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
某化学实验小组为测定生石膏的组成,即测x的值,做了如下实验,将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量,随着实验次数的增加,加热的时间不断延长.它们的实验数据理如下:
利用数据可绘制成以下图象:

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.
| 实验顺序 (按序延长加热时间) | 固体质量/g | |
| 加热前 | 加热后 | |
| 1 | 3.44 | 3.26 |
| 2 | 3.44 | 3.12 |
| 3 | 3.44 | 2.90 |
| 4 | 3.44 | 2.90 |
| 5 | 3.44 | 2.80 |
| 6 | 3.44 | 2.78 |
| 7 | 3.44 | 2.72 |
| 8 | 3.44 | 2.72 |

(1)利用实验数据,通过计算推断生石膏的化学式.
(2)通过计算解释图象中产生AB段的原因.