题目内容
利用氢气还原氧化铜的实验测定水的组成.装置如图所示:
已知氧化铜和玻璃管在通入氢气前的总质量是56 g,在通入氢气完全反应后的总质量为51.2 g,氯化钙和U形管在实验前的总质量是104.6 g,在实验后的总质量是110 g求:

(1)完全反应后生成水的质量;
(2)生成的水中氧元素的质量;
(3)生成的水中氢元素的质量;
(4)水中氢、氧元素的质量比;
(5)若已知氢的相对原子质量为1,氧的相对原子质量为16,求水的化学式.
答案:
解析:
解析:
|
答:(略) 解:(1)生成水的质量为:110 g-104.6 g=5.4 g; (2)水中氧元素的质量等于氧化铜通H2后减少的质量:56 g-51.2 g=4.8 g; (3)水中氢元素的质量为:5.4 g-4.8 g=0.6 g; (4)水中氢、氧元素的质量比为:0.6 g∶4.8 g=1∶8; |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
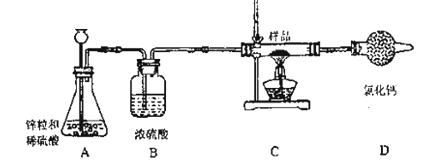
小光在研究性学习中了解到氢气具有还原性。他设计了一个实验,利用氢气的还原性来探究某不纯的氧化铜样品中氧化铜的质量分数(杂质为铜,不与氢气反应),C装置中发生反应的化学方程式为:H2+CuO![]() Cu+H2O
Cu+H2O
友情提示:氯化钙固体可用作干燥剂。装置图如下所示,部分起固定作用的装置未画出。
|
(2)小明同学用同样的装置进行实验,实验结果与小光所得的正确结果比较出现偏差,请分析可能造成误差的原因(写一条即可):
(3)小光是利用氢气还原氧化铜的原理进行测定,请你简要写出其它测定样品中氧化铜的质量分数的方法和要测定的数据(用文字叙述,无需写出具体质量数值)。

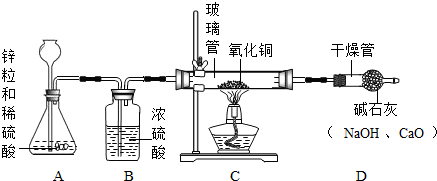

 某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究。
某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究。