题目内容
 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与他们的探究并回答问题.(1)【提出问题】假设l:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;
假设3:红色粉末是
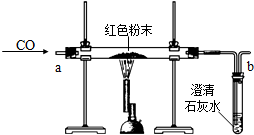
(2)【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置如图所示).
请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 假设1成立 | |
| 假设2成立 | |
| 假设3成立 |
(4)【反思与评价】
①实验过程中,硬质玻璃管内发生反应的化学方程式是
②实验时通入一氧化碳片刻后再加热的原因是
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是
(5)【拓展】根据你最近所学的知识,请再设计一种实验方案确认假设3成立.
| 操作方法 | 预计实验现象 | 有关化学方程式 |
考点:实验探究物质的组成成分以及含量,一氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据题意,对红色粉末进行猜想;
(2)根据实验结论,分析支持结论应该出现的实验现象;
(4)对实验装置的操作进行解释及对存在问题进行改进;
(5)根据氧化铁和铜的化学性质分析选择的试剂.
(2)根据实验结论,分析支持结论应该出现的实验现象;
(4)对实验装置的操作进行解释及对存在问题进行改进;
(5)根据氧化铁和铜的化学性质分析选择的试剂.
解答:解:
(1)该粉末是铜粉和氧化铁粉中的一种或两种,因此红色粉末可能为两物质的混合物;
(2)铜在高温下不与一氧化碳反应,因此粉末不变色,澄清石灰水也不会出现浑浊;氧化铁在高温下可与一氧化碳反应生成黑色铁粉和二氧化碳,充分反应后,粉末变黑色,澄清石灰水浑浊;
(4)①一氧化碳还原氧化铁生成铁和二氧化碳;化学方程式为3CO+Fe2O3
2Fe+3CO2;
②一氧化碳具有可燃性,与空气混合点燃可能发生爆炸,因此应先通一氧化碳,待玻璃管内气体为纯净的一氧化碳时再进行加热,防止形成混合气体而引起爆炸;
③一氧化碳气体有毒,直接排放到空气中会造成空气污染,可把尾气进行燃烧或收集;故可在b处用酒精灯点燃,或用塑料袋(气球)收集;
(5)【拓展】氧化铁可与盐酸反应生成黄色的氯化铁溶液,而铜不能与盐酸反应,故根据最近所学的知识,可再设计一种实验方案确认假设3成立.
故答案为:
(1)铜粉和氧化铁粉的混合物
(2)
(4)①3CO+Fe2O3
2Fe+3CO2
②防止加热时硬质玻璃管发生爆炸
③在b处用酒精灯点燃,或用塑料袋(气球)收集
(5)【拓展】设计一种实验方案确认假设3成立.
(1)该粉末是铜粉和氧化铁粉中的一种或两种,因此红色粉末可能为两物质的混合物;
(2)铜在高温下不与一氧化碳反应,因此粉末不变色,澄清石灰水也不会出现浑浊;氧化铁在高温下可与一氧化碳反应生成黑色铁粉和二氧化碳,充分反应后,粉末变黑色,澄清石灰水浑浊;
(4)①一氧化碳还原氧化铁生成铁和二氧化碳;化学方程式为3CO+Fe2O3
| ||
②一氧化碳具有可燃性,与空气混合点燃可能发生爆炸,因此应先通一氧化碳,待玻璃管内气体为纯净的一氧化碳时再进行加热,防止形成混合气体而引起爆炸;
③一氧化碳气体有毒,直接排放到空气中会造成空气污染,可把尾气进行燃烧或收集;故可在b处用酒精灯点燃,或用塑料袋(气球)收集;
(5)【拓展】氧化铁可与盐酸反应生成黄色的氯化铁溶液,而铜不能与盐酸反应,故根据最近所学的知识,可再设计一种实验方案确认假设3成立.
故答案为:
(1)铜粉和氧化铁粉的混合物
(2)
| 实验中可能出现的现象 | 结论 |
| 红色粉末没有变化,石灰水不浑浊 | 假设1成立 |
| 红色粉末全部变为黑色,石灰水变浑浊 | 假设2成立 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 假设3成立 |
| ||
②防止加热时硬质玻璃管发生爆炸
③在b处用酒精灯点燃,或用塑料袋(气球)收集
(5)【拓展】设计一种实验方案确认假设3成立.
| 操作方法 | 预计实验现象 | 有关化学方程式 |
| 取少量红色粉末放入试管中,加入足量的稀盐酸,震荡 | 部分粉末溶解,溶液呈黄色 | Fe2O3+6HCl═2FeCl3+3H2O |
点评:在使用可燃性气体时,一定要注意检验气体的纯度,不纯的气体在点燃时有可能出现爆炸;可能气体主要有:氢气、一氧化碳、甲烷(天然气).

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
日常生活中用到的下列物质,属于纯净物的( )
| A、降温用的冰水混合物 |
| B、取暖用的煤 |
| C、调味用的食醋 |
| D、炒菜用的铁锅 |
广东部分地区雨水的pH值小于5.6,这些雨水是( )
| A、纯净的雨水 |
| B、中性的雨水 |
| C、碱性的雨水 |
| D、酸性的雨水 |
下列变化属于化学变化的是( )
| A、活性炭吸附毒气 | B、食物腐烂 |
| C、粗盐粉碎 | D、石蜡融化 |
一种医用含钾化合物的水溶液能跟硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.该化合物是( )
| A、KNO3 |
| B、K2CO3 |
| C、KCl |
| D、KOH |
质量守恒定律的适用范围是( )
| A、实验室里发生的反应 |
| B、自然界里发生的反应 |
| C、工业生产中发生的反应 |
| D、在自然界里发生的所有化学反应 |
有一种氯化物,经分析测得其中氯元素的质量分数为47.65%,则这种物质是( )
| A、氯化铜 | B、氯化钡 |
| C、氯化钠 | D、氯化钾 |
通过初中化学的学习,我们可以总结或发现许多具有一定规律性的知识.在下列所给的有关规律的描述中,正确的是( )
| A、实验室制取气体前要检查装置的气密性 |
| B、所有的酸中都一定含有氧元素 |
| C、金属与酸发生置换反应后,溶液的质量都增加 |
| D、酸、碱、盐之间都能发生复分解反应 |
 酚酞是一种酸碱指示剂,它的结构如图所示,则酚酞的化学式为
酚酞是一种酸碱指示剂,它的结构如图所示,则酚酞的化学式为