题目内容
11.如图所示实验操作中,不正确的是( )| A. | 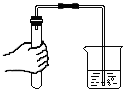 检查气密性 | B. |  读出液体的体积 | C. |  稀释浓硫酸 | D. |  蒸发食盐水 |
分析 A、根据检查装置气密性的方法进行分析判断.
B、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断.
C、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
D、根据蒸发操作的注意事项进行分析判断.
解答 解:A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确
B、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中所示操作正确.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
D、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,图中所示操作正确.
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
6.一般不用K、Ca、Na等活泼金属来置换盐溶液中的其他金属元素,这是教科书上的一句话.小科对此进行了思考,并查阅资料,对金属钠和硫酸铜溶液的反应进行探究.
【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O═2NaOH+H2↑
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成.
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜.
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示
小科咨询老师后得知蓝绿色沉淀为碱式铜盐.
【实验结论】(1)上述实验中均未观察到红色固体生成,由此判断猜想一错误.
(2)实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误.
【实验反思】
(1)实验中生成氢氧化铜沉淀的原理是生成的氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀.
(2)由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有钠块的大小、硫酸铜溶液的浓度.
(3)为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热.
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热.
请从两个方案中选出合理的方案,并说明理由.方案二;隔绝空气加热,能避免钠在空气中被氧化.
【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O═2NaOH+H2↑
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成.
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜.
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示
| 实验编号 | 钠块大小 | 硫酸铜溶液 | 实验中产生沉淀的现象 |
| ① | 绿豆大小 | 稀溶液10ml | 产生蓝绿色沉淀 |
| ② | 绿豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀 |
| ③ | 豌豆大小 | 稀溶液10ml | 产生蓝色絮状沉淀 |
| ④ | 豌豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀,并出现黑色固体 |
【实验结论】(1)上述实验中均未观察到红色固体生成,由此判断猜想一错误.
(2)实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误.
【实验反思】
(1)实验中生成氢氧化铜沉淀的原理是生成的氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀.
(2)由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有钠块的大小、硫酸铜溶液的浓度.
(3)为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热.
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热.
请从两个方案中选出合理的方案,并说明理由.方案二;隔绝空气加热,能避免钠在空气中被氧化.
19.ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )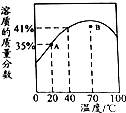

| A. | 40℃时,ZnSO4的溶解度为41g | |
| B. | 点B对应的ZnSO4溶液升温或降温均能达到饱和 | |
| C. | 点A对应的ZnSO4溶液是不饱和溶液 | |
| D. | ZnSO4饱和溶液的溶质质量分数随温度升高而增大 |
6.向AgNO3溶液中加入一定质量Fe和Zn的混合物,充分反应后过滤,得到滤渣和浅绿色滤液.下列说法正确的是( )
| A. | 滤液中一定含有Fe2+、Ag+ | B. | 滤液中一定含有Zn2+、Fe2+ | ||
| C. | 滤渣中一定含有Fe、Ag | D. | 滤渣中一定含有Zn、Ag |
16.下列有关金属材料说法错误的是( )
| A. | 黄铜的硬度比纯铜的硬度小 | |
| B. | 铝具有密度小和抗腐蚀性好的性能 | |
| C. | 铁制品与空气中的氧气、水蒸气接触容易生锈 | |
| D. | 金的化学性质很不活泼,在自然界中有单质的形式存在 |
3.下列实验中无明显现象的是( )
| A. | 向NaOH溶液中通入CO2 | B. | 向CaO中滴加蒸馏水 | ||
| C. | 向Fe2(SO4)3溶液中滴加NaOH溶液 | D. | 向BaCO3中滴加稀HNO3 |
20.向氧化铜和铁粉的混合物中,加入一定量的稀硫酸,反应停止后,过滤,除去不溶物.再向滤液中加一铁片,未看到铁片有任何变化.下列分析正确的是( )
| A. | 滤液中可能含有CuSO4和FeSO4 | B. | 滤液中一定不含有FeSO4和H2SO4 | ||
| C. | 滤出的不溶物中一定含有Cu | D. | 滤出的不溶物中一定含有Cu和Fe |
1.下列是生活中常见的一些变化,其中属于化学变化的是( )
| A. | 春天花香四溢 | B. | 洗涤剂可以去油污 | ||
| C. | 水力、风力发电 | D. | 蚊虫叮咬后涂抹肥皂水 |