题目内容
有下列两种金属组成的混合物2.5g,放入足量的稀硫酸中,充分反应后得到氢气0.1g,则该金属的组合应该是
- A.Mg Al
- B.Fe Cu
- C.Al Zn
- D.Fe Zn
C
以产生2gH2进行判断,假设金属混合物为M.
MH2M2
2.5 g0.1 g
M∶2=2.5 g∶0.1 gM=50
以上说明:产生2 g氢气需要50 g混合金属,所以只有当组成混合物的金属中产生2 gH2时所需要的金属一个大于50 g,另一个小于50 g,才能够平均为50 g.
以产生2 gH2为标准时,需要Mg:24 g,Al:18 g,Cu:+∞,Fe:56 g,Zn:65 g.
不难找出,只有C符合条件.
以产生2gH2进行判断,假设金属混合物为M.
MH2M2
2.5 g0.1 g
M∶2=2.5 g∶0.1 gM=50
以上说明:产生2 g氢气需要50 g混合金属,所以只有当组成混合物的金属中产生2 gH2时所需要的金属一个大于50 g,另一个小于50 g,才能够平均为50 g.
以产生2 gH2为标准时,需要Mg:24 g,Al:18 g,Cu:+∞,Fe:56 g,Zn:65 g.
不难找出,只有C符合条件.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
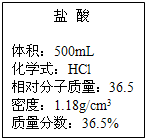 实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题.
实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题. 实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题.
实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题.