题目内容
10.下列五种溶液:①NaOH溶液、②Ba(OH)2溶液、③Na2SO4溶液、④稀硝酸、⑤混有少量硝酸的MgSO4溶液.(1)指出其中属于碱溶液的是①②(选填序号);
(2)若要配置100克5%的硫酸钠溶液,需要往20%的硫酸钠溶液中加水多少克?75g.
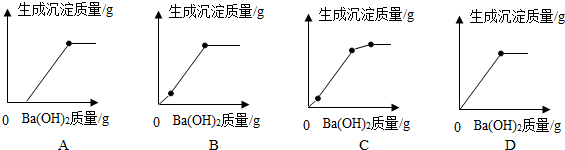
(3)若将Ba(OH)2溶液逐滴加入到混有少量硝酸的MgSO4溶液中,所得沉淀的质量与加入的Ba(OH)2的质量变化符合下列图象的是C(选填字母序号).
分析 根据物质的性质、溶液稀释前后溶质质量不变、物质反应生成沉淀与图象的关系进行分析解答即可.
解答 解:(1)氢氧化钠、氢氧化钡属于碱的溶液,故填:①②;
(2)设20%的硫酸钠溶液的质量为x,则有:100g×5%=20%x,x=25g,故加水的质量为:100g-25g=75g,故填:75g;
(3)将Ba(OH)2溶液逐滴加入到混有少量硝酸的MgSO4溶液中,钡离子与硫酸根离子结合就产生沉淀,故沉淀从0开始就产生,当硝酸完全反应后,氢氧根离子与镁离子结合产生沉淀,故沉淀的质量会增大,故图C符合,故填:C.
点评 本题考查的是常见的物质的性质以及溶液的有关计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20. 化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
 化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )| A. | 计算所需水的质量为200g | |
| B. | 按照图示步骤量取水,配置的溶液质量分数将偏小 | |
| C. | 实验室有10mL、50mL、100mL规格的量筒,量取浓硫酸应选择100mL的量筒 | |
| D. | 将浓硫酸沾到皮肤上,应立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液 |
1.下列物质中,能作钾肥的是( )
| A. | NH4H2PO4 | B. | NH4HCO3 | C. | CO(NH2)2 | D. | KCl |
18.下列事实和相应的解释不一致的是( )
| 选项 | 事实 | 解释 |
| A | 敞口放置的浓盐酸逐渐变稀 | 分子在不断地运动 |
| B | 用汽油除去衣服上的油污 | 汽油能溶解油污 |
| C | 用二氧化碳灭火器灭火 | 二氧化碳不能燃烧 |
| D | 酒精、水各10mL混匀后体积小于20mL | 分子之间有间隔 |
| A. | A | B. | B | C. | C | D. | D |
5. 月球氦-3含量和分别是我们探月工程的一个重要项目,如图是氦-3原子结构示意图,根据该图,我们不能获得的信息是( )
月球氦-3含量和分别是我们探月工程的一个重要项目,如图是氦-3原子结构示意图,根据该图,我们不能获得的信息是( )
 月球氦-3含量和分别是我们探月工程的一个重要项目,如图是氦-3原子结构示意图,根据该图,我们不能获得的信息是( )
月球氦-3含量和分别是我们探月工程的一个重要项目,如图是氦-3原子结构示意图,根据该图,我们不能获得的信息是( )| A. | 氦-3原子的核外电子数 | B. | 氦-3原子的中子数 | ||
| C. | 氦-3原子的核电荷数 | D. | 氦-3原子的体积大小 |
2.根据实验要求,分析作答.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:
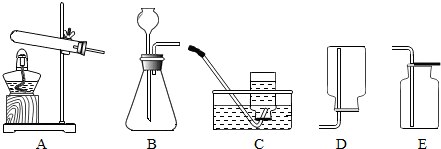
①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:
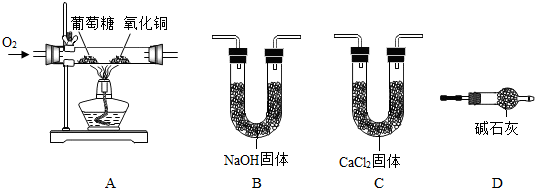
①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
反应中生成水的质量是n-mg.(用M、N或m、n表示)
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:

①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:

①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
| 装置 | 反应前装置的质量/g | 反应后装置的质量/g |
| B | M | N |
| C | m | n |
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
19.下列对分子的认识,说法不正确的是( )
| A. | 墙内开花墙外香,说明分子在不停地运动 | |
| B. | “破镜不能重圆”,说明分子间有斥力 | |
| C. | 水与酒精混合后总体积变小,说明分子间有间隔 | |
| D. | 一氧化碳、二氧化碳的化学性质不同,是因为它们分子的构成不同 |
8.下列有关化肥的说法不正确的是( )
| A. | 氨肥能促进植物枝叶茂盛,叶色浓绿 | |
| B. | KNO3属于复合肥 | |
| C. | 尿素[CO(NH2)2]不能与碱性物质混合施用 | |
| D. | 磷肥大多不溶于水 |
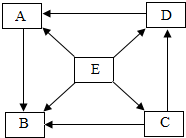 如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.
如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.