题目内容
学习知识的目的之一是分析和解决实际的问题.
(1)为防止资源浪费,燃烧时通常将煤块变为粉末状,其原因是 .
(2)在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体.制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,制取过程中发生反应的化学方程式为 .
(3)CaCl2溶液和NaHCO3溶液反应生成CaCO3.为表示这个反应写出了下列两个化学方程式:
①CaCl2+NaHCO3═CaCO3↓+NaCl+HCl;②CaCl2+2NaHCO3═CaCO3↓+2NaCl+CO2↑+H2O
你认为化学方程式 不合理,请简述理由 .
(1)为防止资源浪费,燃烧时通常将煤块变为粉末状,其原因是
(2)在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体.制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,制取过程中发生反应的化学方程式为
(3)CaCl2溶液和NaHCO3溶液反应生成CaCO3.为表示这个反应写出了下列两个化学方程式:
①CaCl2+NaHCO3═CaCO3↓+NaCl+HCl;②CaCl2+2NaHCO3═CaCO3↓+2NaCl+CO2↑+H2O
你认为化学方程式
考点:完全燃烧与不完全燃烧,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律,化学与生活
分析:(1)促进可燃物燃烧的方法有:增大可燃物与氧气的接触面积或增大氧气的浓度,据此进行分析解答.
(2)根据题意,制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,写出反应的化学方程式即可.
(3)根据复分解反应及其发生的条件:若两种物质相互交换成分有沉淀、气体或水生成,则能发生化学反应,判断反应是否合理.
(2)根据题意,制取轻质碳酸钙粉末是用净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,写出反应的化学方程式即可.
(3)根据复分解反应及其发生的条件:若两种物质相互交换成分有沉淀、气体或水生成,则能发生化学反应,判断反应是否合理.
解答:解:(1)燃烧时通常将煤块变为粉末状,增大煤与氧气(或空气)的接触面积,使煤充分燃烧.
(2)根据题意结合所学知识,氢氧化钙能与二氧化碳反应生成碳酸钙和水,反应的化学方程式为CO2+Ca(OH)2 ═CaCO3↓+H2O.
(3)因CaCl2+NaHCO3═CaCO3↓+NaCl+HCl反应的生成物中CaCO3能与HCl反应,则该反应不合理;而CaCl2+2NaHCO3═CaCO3↓+2NaCl+CO2↑+H2O反应有沉淀和气体、水生成,则该反应合理.
故答案为:(1)增大与氧气(或空气)的接触面积,使其充分燃烧;(2)CO2+Ca(OH)2 ═CaCO3↓+H2O;(3)①;生成物中的CaCO3与HCl不能共存,会发生反应.
(2)根据题意结合所学知识,氢氧化钙能与二氧化碳反应生成碳酸钙和水,反应的化学方程式为CO2+Ca(OH)2 ═CaCO3↓+H2O.
(3)因CaCl2+NaHCO3═CaCO3↓+NaCl+HCl反应的生成物中CaCO3能与HCl反应,则该反应不合理;而CaCl2+2NaHCO3═CaCO3↓+2NaCl+CO2↑+H2O反应有沉淀和气体、水生成,则该反应合理.
故答案为:(1)增大与氧气(或空气)的接触面积,使其充分燃烧;(2)CO2+Ca(OH)2 ═CaCO3↓+H2O;(3)①;生成物中的CaCO3与HCl不能共存,会发生反应.
点评:本题难度不大,掌握使燃料完全燃烧的方法、化学方程式的书写、复分解反应及其发生的条件等是正确解答本题的关键.

练习册系列答案
相关题目
下列物质中,属于纯净物的是( )
A、 矿泉水 |
B、 蒸馏水 |
C、 白醋 |
D、 苏打水 |
如表数据是一些物质的pH,其中一定呈酸性的是( )
| 物质 | 牙膏 | 矿泉水 | 苹果汁 | 肥皂水 |
| pH | 8~9 | 6.5~7.5 | 2.9~3.3 | 9.8~10.2 |
| A、牙膏 | B、矿泉水 |
| C、苹果汁 | D、肥皂水 |
一包不纯的Na2CO3固体,杂质可能是CaCl2、NaCl、NaHCO3中的一种或几种.现取该样品溶于水得到澄清溶液;另取样品10.6g,加入100g稀盐酸恰好完全反应,产生气体4g,则下列判断不正确的是( )
| A、加水得澄清溶液,样品中一定没有CaCl2 |
| B、样品中一定含有NaCl,可能含有NaHCO3 |
| C、样品中一定含有NaHCO3,可能含有NaCl |
| D、所加的稀盐酸溶质质量分数小于7.3% |

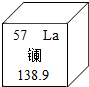 氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法正确的是
氢是新型清洁能源,但难储运.研究发现,镧和镍的一种合金是储氢材料.下列有关57号元素镧(La)的说法正确的是