题目内容
石灰石、生石灰和熟石灰在日常生活中有多种用途,请在下表中写出有关的化学方程式,并回答有关的问题:| 用途 | 化学方程式 | 相关问题 |
| 用石灰石制生石灰 | __________ | 反应类型:__________ |
| 生石灰常用作某些食品的干燥剂 | __________ | 此反应____(填“吸吸热”或“放热”) |
| 用熟石灰降低含有少量硫酸的污水的酸性 | __________ | 这是中和反应在实际中的应用. |
该反应的化学方程式为:CaCO3
| ||
该反应由一种物质反应生成两种物质,符合分解反应的概念,属于分解反应.
氧化钙与水反应生成氢氧化钙.
该反应的化学方程式为:CaO+H2O=Ca(OH)2.
该反应中放出大量的热.
氢氧化钙与硫酸反应生成硫酸钙和水.
该反应由酸和碱反应生成盐和水,符合中和反应的概念.
该反应的化学方程式为:Ca(OH)2+H2SO4=CaSO4+2H2O.
故答案为:
CaCO3
| ||
CaO+H2O=Ca(OH)2;放热.
Ca(OH)2+H2SO4=CaSO4+2H2O.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案.(10分)2011年9月,某牙膏被曝含有致癌物“三氯生”而引起消费者的焦虑,于是同学们开展了对牙膏成分及作用的探究,经过查阅资料得知:
(1)很多品牌牙膏都标有“含氟”字样,其中的“氟”是指
A.氟单质 B.氟元素 C.氟原子
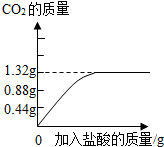
(2)牙膏去污主要是利用了摩擦作用。某品牌牙膏中的摩擦剂是碳酸钙,为了检验并测定牙膏中碳酸钙的质量分数,同学们取了10g牙膏,加入足量稀盐酸并搅拌。实验过程中记录并处理数据形成下图曲线:

该品牌牙膏中碳酸钙的质量分数为多少。
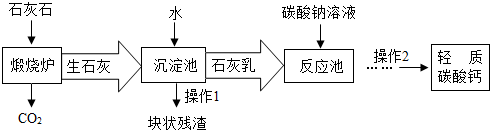
(3)用作牙膏摩擦剂的轻质碳酸钙可以石灰石来制备,工业上主要生产流程如下:

①“煅烧炉”中发生反应的化学方程式是: ,在“反应池”中主要发生反应的化学方程式是: 。
②“沉淀池”中生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆,熟石灰浆为
(选填“悬浊液”或“溶液”或“乳浊液”)。
③有人建议在上述流程中用CO2替代“碳酸钠溶液”。这样做的优点是 。
小王查阅资料后得知:a.二氧化碳持续通入氢氧化钙溶液发生如下反应: CO2+Ca(OH)2=CaCO3↓+H2O, CaCO3+ H2O + CO2=Ca(HCO3)2;
|
为了防止利用该法制得的轻质碳酸钙中混有Ca(HCO3)2,操作2中必需要进行的一步操作是 。
【解析】(1)运用物质是由元素组成的,“含氟”字样,其中的“氟”是指氟元素解答.
(2)由图可知碳酸钙和盐酸完全反应后生成的二氧化碳质量为1.32g,根据化学方程式列比例式求出碳酸钙的质量,进行解答
(3)煅烧炉中主要发生的是碳酸钙在高温下分解为氧化钙和二氧化碳的反应,根据化学方程式的书写规则正确书写;
沉淀池中主要发生的是氧化钙与水反应生成氢氧化钙的反应,根据化学方程式的书写规则正确书写;
根据悬浊液和乳浊液的定义进行分析回答;
用二氧化碳代替碳酸钠溶液,可达到降低生产成本和节能减排;
 (2012?玄武区二模)2011年9月,某牙膏被曝含有致癌物“三氯生”而引起消费者的焦虑,于是同学们开展了对牙膏成分及作用的探究,经过查阅资料得知:
(2012?玄武区二模)2011年9月,某牙膏被曝含有致癌物“三氯生”而引起消费者的焦虑,于是同学们开展了对牙膏成分及作用的探究,经过查阅资料得知: