题目内容
(2010?广州)在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来.(1)CuSO4溶液中,大量存在的离子是.
(2)将铝丝浸入CuSO4溶液中,静置,观察到的现象是.结合现象分析,溶液中减少的离子是,增加的离子是.
(3)除硫酸铜溶液外,将铝丝浸入(任举一例)溶液中,也能产生相同的实验现象.
【答案】分析:(1)根据电离的知识,分析溶液中的离子;
(2)根据金属与盐溶液的反应,推断反应可能出现的实验现象;并分析溶液中离子的变化;
(3)由实验现象,分析置换反应所使用的盐溶液.
解答:解:(1)硫酸铜溶于水,在水的作用下硫酸铜电离成铜离子和硫酸根离子,因此溶液中大量存在铜离子和硫酸根离子;
故选Cu2+、SO42-;
(2)金属铝的活动性比铜强,铝放入硫酸铜溶液中,铝把溶液中的溶液中铜离子置换为铜附着在金属铝表面,溶液逐渐变成硫酸铝的无色溶液,金属铝变成铝离子;
故答案为:铝丝上有红色固体生成,溶液颜色变浅(或溶液由蓝色变为无色);Cu2+;Al3+;
(3)若产生相同的实验现象,则盐溶液应为铜盐,可溶性铜盐还有氯化铜、硝酸铜等;
故选CuCl2[或Cu(NO3)2].
点评:铝与硫酸铜溶液的置换反应,其实质是较活泼金属单质铝把溶液的活动性弱的金属铜的离子置换成金属单质铜的过程,反应通过电子转移实现金属间原子与离子的转换.
(2)根据金属与盐溶液的反应,推断反应可能出现的实验现象;并分析溶液中离子的变化;
(3)由实验现象,分析置换反应所使用的盐溶液.
解答:解:(1)硫酸铜溶于水,在水的作用下硫酸铜电离成铜离子和硫酸根离子,因此溶液中大量存在铜离子和硫酸根离子;
故选Cu2+、SO42-;
(2)金属铝的活动性比铜强,铝放入硫酸铜溶液中,铝把溶液中的溶液中铜离子置换为铜附着在金属铝表面,溶液逐渐变成硫酸铝的无色溶液,金属铝变成铝离子;
故答案为:铝丝上有红色固体生成,溶液颜色变浅(或溶液由蓝色变为无色);Cu2+;Al3+;
(3)若产生相同的实验现象,则盐溶液应为铜盐,可溶性铜盐还有氯化铜、硝酸铜等;
故选CuCl2[或Cu(NO3)2].
点评:铝与硫酸铜溶液的置换反应,其实质是较活泼金属单质铝把溶液的活动性弱的金属铜的离子置换成金属单质铜的过程,反应通过电子转移实现金属间原子与离子的转换.

练习册系列答案
相关题目
(2010广州29)某校科技节有如下挑战项目:通过实验鉴别两种无色溶液和两种黑色粉末,已知它们分别是稀硫酸、硫酸钠溶液以及氧化铜和铁中的一种。现场仅提供了紫色石蕊试液、碳酸钠溶液、氢氧化钠溶液以及常用的实验仪器。
请设计一个完成该挑战项目的实验方案,写出实验步骤、预期现象与结论。
| 实验步骤 | 预期现象与结论 |
|
|
|
|
|
|
(2010义乌33.) 2010年5月12日,在苍茫海水中沉没了800多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑。已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:
某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比。
实验用到的主要装置为:
装置连接顺序为: __ 。(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表;
根据以上数据可得产生的水和二氧化碳的质量之比为 __ __ 。(要求写出最简整数比)
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些? __ __
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解
(2010?广州)铁、铝、铜是日常生活中使用最广泛的金属.
(1)上述三种金属中,人类最早大规模冶炼和使用的是铜,最晚的是铝,原因是(填序号).
A.三者在地壳中的含量,铜元素最高,铝元素最低
B.三者的金属活动性,铜元素最弱,铝元素最强
C.在自然界中,铜元素主要以单质形式存在,铝元素以化合物形式存在
(2)常温下一些金属的物理性质数据如下:
分析上述数据,碎石用的大锤常用铁制而不用铝制,原因是
.
(3)铜器长期暴露在空气中,表面会生成铜绿[其成分可表示为Cu2(OH)2CO3],从其组成分析,预测铜绿能与(任举一例)反应.
(4)工业上火法炼铜的一个主要反应是Cu2S+O2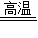 2Cu+SO2.Cu2S中铜元素的质量分数为.用500吨含Cu2S 80%的铜矿石,理论上可以炼出吨铜.
2Cu+SO2.Cu2S中铜元素的质量分数为.用500吨含Cu2S 80%的铜矿石,理论上可以炼出吨铜.
(1)上述三种金属中,人类最早大规模冶炼和使用的是铜,最晚的是铝,原因是(填序号).
A.三者在地壳中的含量,铜元素最高,铝元素最低
B.三者的金属活动性,铜元素最弱,铝元素最强
C.在自然界中,铜元素主要以单质形式存在,铝元素以化合物形式存在
(2)常温下一些金属的物理性质数据如下:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g?cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
.
(3)铜器长期暴露在空气中,表面会生成铜绿[其成分可表示为Cu2(OH)2CO3],从其组成分析,预测铜绿能与(任举一例)反应.
(4)工业上火法炼铜的一个主要反应是Cu2S+O2
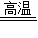 2Cu+SO2.Cu2S中铜元素的质量分数为.用500吨含Cu2S 80%的铜矿石,理论上可以炼出吨铜.
2Cu+SO2.Cu2S中铜元素的质量分数为.用500吨含Cu2S 80%的铜矿石,理论上可以炼出吨铜.