题目内容
某同学在实验室发现一包白色粉末.他将该粉末取少量放入试管中,滴入稀盐酸,有气泡产生.请你参与并帮助完成下列探究活动:
(1)提出问题:该气体的成分是什么?
(2)猜想与假设:该气体可能是CO2
(3)设计与实验:
老师告诉他:该白色粉末是Na2CO3、K2CO3、CaCO3、BaCO3中的两种,于是该同学做了进一步探究.
(4)提出问题:该白色粉末的成分是什么?
(5)猜想与假设:
猜想1:该白色粉末若能完全溶于水,则它是Na2CO3和K2CO3(填化学式);
猜想2:该白色粉末若完全不能溶于水,则它是CaCO3和
(6)设计与实验:
①取白色粉末少许于试管中,再注入适量水,振荡,粉末全部溶解.
②向①中滴入澄清石灰水,溶液中出现白色沉淀.
(7)实验结论:猜想
(1)提出问题:该气体的成分是什么?
(2)猜想与假设:该气体可能是CO2
(3)设计与实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用一支玻璃棒蘸取少许澄清石灰水,放在产生气体的试管口 | 玻璃棒上有白色物质产生 | 化学方程式: Ca(OH)2+CO2═CaCO3↓+H2O Ca(OH)2+CO2═CaCO3↓+H2O .该气体是CO2,由此可判断该白色粉末中含有 碳酸 碳酸 盐. |
(4)提出问题:该白色粉末的成分是什么?
(5)猜想与假设:
猜想1:该白色粉末若能完全溶于水,则它是Na2CO3和K2CO3(填化学式);
猜想2:该白色粉末若完全不能溶于水,则它是CaCO3和
BaCO3
BaCO3
(填化学式).(6)设计与实验:
①取白色粉末少许于试管中,再注入适量水,振荡,粉末全部溶解.
②向①中滴入澄清石灰水,溶液中出现白色沉淀.
(7)实验结论:猜想
1
1
正确.请你思考判断:该同学做的上述实验中,没有
没有
(填:“有”或“没有”)必要做第②步,理由是因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水
因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水
.分析:(3)根据二氧化碳与氢氧化钙反应考虑;(5)根据白色粉末物质的溶解性分析(7)根据Na2CO3、K2CO3、CaCO3、BaCO3的溶解性考虑.
解答:解:(3)二氧化碳能使澄清石灰水变浑浊,反应物是氢氧化钙和二氧化碳,生成物是碳酸钙和水,化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;由此判断该白色粉末中含有碳酸盐
(5)白色粉末是Na2CO3、K2CO3、CaCO3、BaCO3中碳酸钙和碳酸钡难溶于水
(7)取白色粉末少许于试管中,再注入适量水,振荡,粉末全部溶解,说明该粉末易溶于水,因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水,就可说明猜想1正确.没有必要做第②步.
故答案为:
(3)Ca(OH)2+CO2═CaCO3↓+H2O 碳酸
(5)BaCO3
(7)1 没有 因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水.
(5)白色粉末是Na2CO3、K2CO3、CaCO3、BaCO3中碳酸钙和碳酸钡难溶于水
(7)取白色粉末少许于试管中,再注入适量水,振荡,粉末全部溶解,说明该粉末易溶于水,因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水,就可说明猜想1正确.没有必要做第②步.
故答案为:
(3)Ca(OH)2+CO2═CaCO3↓+H2O 碳酸
(5)BaCO3
(7)1 没有 因为CaCO3、BaCO3属于沉淀,Na2CO3、K2CO3都易溶于水.
点评:解答本题要注意方程式的书写方法,知道常见物质在水中的溶解性.

练习册系列答案
相关题目
 某同学在实验室发现一瓶标签残缺(如下图所示)的溶液.为了测定此溶液的溶质质量分数,他取出100g该溶液,向其中逐渐滴加溶质质量分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.
某同学在实验室发现一瓶标签残缺(如下图所示)的溶液.为了测定此溶液的溶质质量分数,他取出100g该溶液,向其中逐渐滴加溶质质量分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.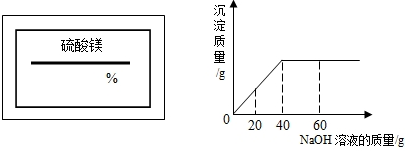
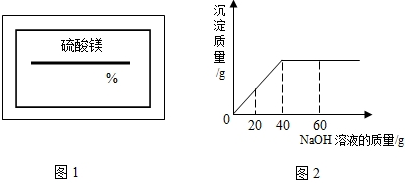
 (2009?南开区一模)某同学在实验室发现一瓶标签残缺的硫酸镁溶液.为了测定此溶液的溶质质量分数,他取出25g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.试求:
(2009?南开区一模)某同学在实验室发现一瓶标签残缺的硫酸镁溶液.为了测定此溶液的溶质质量分数,他取出25g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.试求: (2008?金城江区)某同学在实验室发现一瓶标签残缺(如图所示)的溶液.为了测定此溶液的溶质质量分数,他取出20g该溶液,向其中逐滴加入溶质质量分数为15%的MgSO4溶液,反应过程中生成沉淀的质量与所用MgSO4溶液质量的关系如图所示.请计算此溶液的溶质质量分数.
(2008?金城江区)某同学在实验室发现一瓶标签残缺(如图所示)的溶液.为了测定此溶液的溶质质量分数,他取出20g该溶液,向其中逐滴加入溶质质量分数为15%的MgSO4溶液,反应过程中生成沉淀的质量与所用MgSO4溶液质量的关系如图所示.请计算此溶液的溶质质量分数.