题目内容
向50.0g 8.0%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液pH=7.
(1)求反应前氢氧化钠溶液中溶质的质量
(2)求反应后生成硫酸钠的质量。
(1)求反应前氢氧化钠溶液中溶质的质量
(2)求反应后生成硫酸钠的质量。
解:(1)氢氧化钠的质量=50.0g×8.0%=4.0g
(2)设反应后溶液中硫酸钠的质量为x
H2SO4 + 2NaOH == Na2SO4 + 2H2O
80 142
4.0g x
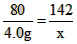
x=7.1g
(2)设反应后溶液中硫酸钠的质量为x
H2SO4 + 2NaOH == Na2SO4 + 2H2O
80 142
4.0g x
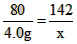
x=7.1g

练习册系列答案
相关题目
 (2012?高新区二模)某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
(2012?高新区二模)某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
 (1)汽车尾气处理相关反应为:2NO+2CO→N2+2CO2,
(1)汽车尾气处理相关反应为:2NO+2CO→N2+2CO2,