题目内容
5. 某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取5片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为55.6g.
某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取5片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为55.6g.(提示:CaCO3+2HCl=CaCl2+H2O+CO2↑)
(1)5片钙片共10g,反应中生成4.4g二氧化碳.
(2)通过计算说明实际含钙量是否与标注相符.
分析 根据质量守恒定律可知,前后总质量变化是因为生成了二氧化碳,所以可求二氧化碳的质量,进而求算碳酸钙的质量或者直接根据关系式法求算出钙元素的质量.
解答 解:五片钙片的质量为2g/片×5=10g,根据质量守恒定律可知,生成的二氧化碳的质量为10g+50g-55.6g=4.4g
设五片钙片对应的钙元素的质量为x.
根据CaCO3+2HCl=CaCl2+H2O+CO2↑和碳酸钙的化学式可得
Ca----CaCO3--------CO2↑
40 44
x 4.4g
$\frac{40}{44}$=$\frac{x}{4.4g}$
x=4g.
则每片钙片的含钙量为$\frac{4g}{5}$=0.8g>0.6g
实际含钙量与标注相符
答:(1)5片钙片共 10g,反应中生成 4.4g二氧化碳.
(2)通过计算说明实际含钙量与标注相符.
点评 计算过程中要灵活,本题可以先计算碳酸钙,然后结合化学式计算钙元素,但是也可以直接根据关系式求算钙元素的质量,从而减少计算的过程.

练习册系列答案
相关题目
13.下列变化与其它三种变化有本质的区别的是( )
| A. | 铁生锈 | B. | 食物腐烂 | C. | 煤燃烧 | D. | 水汽化 |
17.下列物质中含有氧分子的是( )
| A. | 二氧化碳 | B. | 空气 | C. | 氧化镁 | D. | 臭氧 |
14.化学实验是进行科学探究的重要途径,规范的实验操作是科学探究活动的基础和保证.以下图示正确的是( )
| A. | 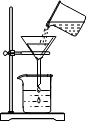 过滤 | B. |  加入块状固体 | C. |  滴加液体 | D. |  倾倒液体 |
15.实验室用高锰酸钾制取氧气的步骤如下:①装药品在试管中,塞紧单孔塞②收集气体③检验装置气密性④灭酒精灯⑤固定试管在铁架台上⑥导管出水槽⑦酒精灯加热药品.正确的操作顺序是( )
| A. | ②③⑤⑥⑦④ | B. | ③①⑤⑦②⑥④ | C. | ①③④⑤⑥⑦② | D. | ③①⑤⑦②④⑥ |

 如图是电解水的示意图.
如图是电解水的示意图.