题目内容
13.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将80g 该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )| A. | 12.8g | B. | 18g | C. | 13.2g | D. | 20g |
分析 因为反应后减少的是二氧化碳,钙元素全部转化为CaO中的钙,则只要计算出所有CaO中的钙元素即可求出.
解答 解:80g混合物含钙元素的质量=80g×60%=48g,反应后氧化钙中钙元素的质量也为48g,高温煅烧生成氧化钙的质量:48g÷($\frac{40}{56}$×100%)=67.2g,故产生的二氧化碳质量:80g-67.2g=12.8g.
故选:A.
点评 本题考查元素的质量分数计算,学生利用碳酸钙完全分解后固体为氧化钙,再利用钙元素的质量守恒来推断生成氧化钙的质量是解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.如表列出了部分人体中含量较多元素的原子结构示意图.请回答下列问题.
(1)属于第四周期的元素是K、Ca.
(2)钙元素的核电荷数是20,若某种该原子的相对原子质量为40,则它的中子数为20.
(3)一般来说,金属元素的原子最外层电子数目<(填“<”、“=”或“>”)4个;钠、钾的化学性质有许多相似之处,其原因是原子的最外层电子数相同.
(4)比较下列三种微粒的架构,找出相同点和不同点.

①相同点电子层结构相同;(写出其中一点即可)
②不同点核电荷数不同.(写出其中一点即可)
| H | O | Na | Mg | Cl | K | Ca |
 |  |  |  |  |  |  |
(2)钙元素的核电荷数是20,若某种该原子的相对原子质量为40,则它的中子数为20.
(3)一般来说,金属元素的原子最外层电子数目<(填“<”、“=”或“>”)4个;钠、钾的化学性质有许多相似之处,其原因是原子的最外层电子数相同.
(4)比较下列三种微粒的架构,找出相同点和不同点.

①相同点电子层结构相同;(写出其中一点即可)
②不同点核电荷数不同.(写出其中一点即可)
18.我们每时每刻都离不开空气.空气中含量最多的气体是( )
| A. | O2 | B. | CO2 | C. | 稀有气体 | D. | N2 |
5.阿司匹林的化学式为C9H8O4.下列关于阿司匹林的说法不正确的是( )
| A. | 阿司匹林由碳、氢、氧三种元素组成 | |
| B. | 1个阿司匹林分子由9个碳原子、8个氢原子、4个氧原子构成 | |
| C. | 阿司匹林中氢、氧元素的质量比为1:8 | |
| D. | 阿司匹林中氧元素的质量分数最小 |
2.如图是A、B、C三种固体物质的溶解度曲线,下列分析不正确的是( )


| A. | 50℃时,三种物质的溶解度由大到小的顺序是A>B>C | |
| B. | 20℃时,A和C两种物质的溶解度相等 | |
| C. | 50℃时,100gA的饱和溶液中,溶质质量为50g | |
| D. | 分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是B>A>C |
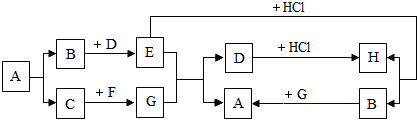
 A-K为初中化学常见的物质,其中A为黑色物质,H是一种建筑材料的主要成分,它们之间的转化关系如图所示.
A-K为初中化学常见的物质,其中A为黑色物质,H是一种建筑材料的主要成分,它们之间的转化关系如图所示.