题目内容
【题目】利用如图所示装置可以进行金属性质的探究。

(1)若装置A中盛放硫酸铜溶液,可观察到什么现象?
(2)若将铁片浸入装置A的溶液中,观察到铁片表面有气泡产生,写出有关反应的化学方程式(写出一个即可)。
(3)利用装置B探究Fe、Cu、Ag三种金属的活动性顺序时,装置B中金属片和溶液中的溶质应分别选择什么物质(写出一组即可)?
【答案】(1)铁表面有红色固体析出,一段时间后,溶液由蓝色变为浅绿色 (2)Fe+2HCl=== FeCl2 + H2↑(合理即可) (3)金属片为铁片和银片,溶液为CuSO4溶液
【解析】(1)铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,可观察到铁片表面有红色物质生成,一段时间后溶液由蓝色变为浅绿色;(2)铁能与酸反应生成盐和氢气,若将铁片浸入装置A的溶液中,观察到铁片表面有气泡产生,说明A是酸,可能是稀盐酸或稀硫酸,铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式是Fe+2HCl=FeCl2+H2↑(或Fe+H2SO4=FeSO4+H2↑);(3)在验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应,装置B中金属片和溶液中的溶质分别是Fe、Ag、CuSO4。

练习册系列答案
相关题目
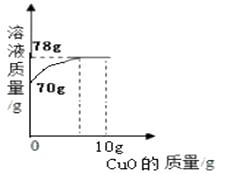
【题目】在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )
序号 | 甲 | 乙 |
A | CuSO4溶液 | 铁粉 |
B | H2SO4溶液 | 锌粒 |
C | HCl溶液 | NaOH溶液 |
D | CaCl2溶液 | Na2CO3溶液 |
A.A
B.B
C.C
D.D