题目内容
物质的颜色是物质的一种重要的物理性质.请写出下列物质的颜色.
木炭
木炭
黑色
黑色
,氧化铜黑色
黑色
,硫酸铜白色
白色
胆矾蓝色
蓝色
,氯酸钾白色
白色
,二氧化锰黑色
黑色
.分析:物质在化学变化中表现出来的性质叫化学性质,物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.木炭是黑色固体,氧化铜、二氧化锰是黑色粉末状的固体;硫酸铜、氯酸钾都是白色固体;硫酸铜晶体的俗名叫胆矾或蓝矾,是蓝色固体.
解答:解:物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性等.木炭是黑色固体,氧化铜、二氧化锰是黑色粉末状的固体;硫酸铜、氯酸钾都是白色固体;硫酸铜晶体的俗名叫胆矾或蓝矾,是蓝色固体故答案为:黑色;黑色;白色;蓝色;白色;黑色;
点评:本考点考查了物理性质和化学性质,要记忆有关的知识点,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
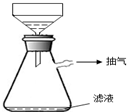 硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录: