题目内容
12.工业上用氢氧化钠溶液吸收工厂排出的二氧化硫气体.请计算:(1)要配制100Kg20%的氢氧化钠溶液,需要20Kg氢氧化钠固体;
(2)若用60Kg30%的氢氧化钠溶液加30Kg水稀释,也可配制20%的氢氧化钠溶液;
(3)用含氢氧化钠8Kg的氢氧化钠溶液吸收二氧化硫气体,理论上可处理二氧化硫气体的质量是多少?(有关反应的化学方程式为:2NaOH+SO2═Na2SO3+H2O)
分析 (1)根据溶质质量等于溶液质量和溶质质量分数的乘积进行分析;
(2)根据稀释前后溶质的质量不变分析解答;
(3)根据反应的化学方程式,结合氢氧化钠的质量计算出可吸收的二氧化硫的质量.
解答 解:(1)配制100Kg20%的氢氧化钠溶液,需要氢氧化钠固体的质量为:100kg×20%=20kg;故填:20;
(2)设需加水的质量为x
60kg×30%=(60+x)kg×20%,解得:x=30kg;故填:30;
(3)设可吸收SO2的质量为x
2NaOH+SO2═Na2SO3+H2O
80 64
8kg x
$\frac{80}{64}=\frac{8kg}{x}$
x=6.4kg
答:理论上可处理二氧化硫气体的质量是6.4kg.
点评 熟练掌握根据化学方程式进行计算的一般步骤,并注意格式.

练习册系列答案
相关题目
3.“珍惜地球资源,改变发展方式”是当今世界的共识.针对这一主题下列表达正确的是( )
| A. | 地球上水含量非常丰富,无需节约,可以任意使用 | |
| B. | 煤、石油、天然气属于可再生资源,取之不尽、用之不竭 | |
| C. | 世界上没有真正的垃圾,只有放错地方的资源 | |
| D. | 大力提倡使用一次性筷子、纸杯等 |
20.有关分子、原子的说法正确的是( )
| A. | 由同种分子构成的物质化学性质相同 | |
| B. | 化学变化中分子、原子都可以分裂 | |
| C. | 分子之间有间隔、原子之间没有间隔 | |
| D. | 分子能构成物质,原子不能直接构成物质 |
7.物质的性质决定用途,下列说法不正确的是( )
| A. | 熟石灰用于改良酸性土壤 | B. | 干冰可以用于人工降雨 | ||
| C. | 碳酸氢钠可以治疗胃酸过多 | D. | 浓硫酸可以作食品干燥剂 |
17.下列洗涤方法中利用了乳化原理的是( )
| A. | 用汽油洗去手上的油污 | B. | 用洗洁精洗去餐具上的油污 | ||
| C. | 用酒精洗去试管中的碘 | D. | 用稀盐酸洗去铁制品表面的铁锈 |
4.下列化学用语与所表述的意义不相符的是( )
| A. | CuO--氧化铜 | |
| B. | 2H2O--2个水分子 | |
| C. | 2H--2个氢元素 | |
| D. | Fe+32O3--氧化铁中铁元素化合价为+3 |

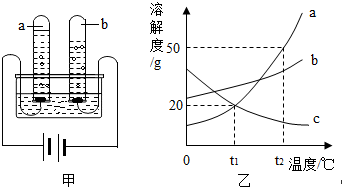 (1)图甲是水通电分解的示意图,在实验过程中,试管a中产生的气体是氧气(填名称).
(1)图甲是水通电分解的示意图,在实验过程中,试管a中产生的气体是氧气(填名称).