题目内容
 (1)人类通过燃烧反应获得的能量,大多来自于煤、
(1)人类通过燃烧反应获得的能量,大多来自于煤、(2)乙醇(C2H5OH)属于可再生能源.乙醇中碳元素、氢元素、氧元素的质量比为
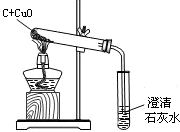
(3)右图是碳和氧化铜在一定条件下进行反应的实验装置,该反应需要几分钟时间.最能说明这个反应已经完成的实验现象是
分析:(1)石油、煤、天然气属于化石燃料,核能、氢能、太阳能等属于新能源;
(2)根据物质的化学式可以进行相关方面的计算;
(3)氧化铜和碳在高温条件下反应能生成铜和二氧化碳.
(2)根据物质的化学式可以进行相关方面的计算;
(3)氧化铜和碳在高温条件下反应能生成铜和二氧化碳.
解答:解:(1)石油、煤、天然气属于化石燃料,核能、氢能等属于新能源.故填:石油;天然气;氢能.
(2)乙醇中碳元素、氢元素、氧元素的质量比为:24:6:16=12:3:8.故填:12:3:8.
4.6g乙醇中含碳元素的质量为:4.6g×
×100%=2.4g.故填:2.4.
(3)最能说明这个反应已经完成的实验现象是导管口不再出现气泡.故填:导管口不再出现气泡.
碳在高温时还原氧化铜的化学方程式为:C+2CuO
2Cu+CO2↑.
解设要使80g氧化铜完全还原,需要碳的质量至少是X,
C+2CuO
2Cu+CO2↑
12 160
X 80g
=
X=6g.故填:6g.
(2)乙醇中碳元素、氢元素、氧元素的质量比为:24:6:16=12:3:8.故填:12:3:8.
4.6g乙醇中含碳元素的质量为:4.6g×
| 24 |
| 46 |
(3)最能说明这个反应已经完成的实验现象是导管口不再出现气泡.故填:导管口不再出现气泡.
碳在高温时还原氧化铜的化学方程式为:C+2CuO
| ||
解设要使80g氧化铜完全还原,需要碳的质量至少是X,
C+2CuO
| ||
12 160
X 80g
| 12 |
| 160 |
| X |
| 80g |
X=6g.故填:6g.
点评:本题主要考查根据物质的化学式、化学方程式计算方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目
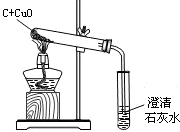 (1)人类通过燃烧反应获得的能量,大多来自于煤、________和________等化石燃料.在开发和使用新能源上也进行了很多尝试.例如,核能、________ 等.
(1)人类通过燃烧反应获得的能量,大多来自于煤、________和________等化石燃料.在开发和使用新能源上也进行了很多尝试.例如,核能、________ 等.

