题目内容
 (1)人类通过燃烧反应获得的能量,大多来自于煤、________和________等化石燃料.在开发和使用新能源上也进行了很多尝试.例如,核能、________ 等.
(1)人类通过燃烧反应获得的能量,大多来自于煤、________和________等化石燃料.在开发和使用新能源上也进行了很多尝试.例如,核能、________ 等.
(2)乙醇(C2H5OH)属于可再生能源.乙醇中碳元素、氢元素、氧元素的质量比为________;4.6g乙醇(C2H5OH)中含碳元素的质量为________g.
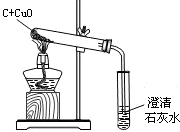
(3)右图是碳和氧化铜在一定条件下进行反应的实验装置,该反应需要几分钟时间.最能说明这个反应已经完成的实验现象是________.碳在高温时还原氧化铜的化学方程式________,要使80g氧化铜完全还原,需要碳的质量至少是________.
解:(1)石油、煤、天然气属于化石燃料,核能、氢能等属于新能源.故填:石油;天然气;氢能.
(2)乙醇中碳元素、氢元素、氧元素的质量比为:24:6:16=12:3:8.故填:12:3:8.
4.6g乙醇中含碳元素的质量为:4.6g× ×100%=2.4g.故填:2.4.
×100%=2.4g.故填:2.4.
(3)最能说明这个反应已经完成的实验现象是导管口不再出现气泡.故填:导管口不再出现气泡.
碳在高温时还原氧化铜的化学方程式为:C+2CuO 2Cu+CO2↑.
2Cu+CO2↑.
解设要使80g氧化铜完全还原,需要碳的质量至少是X,
C+2CuO 2Cu+CO2↑
2Cu+CO2↑
12 160
X 80g
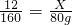
X=6g.故填:6g.
分析:(1)石油、煤、天然气属于化石燃料,核能、氢能、太阳能等属于新能源;
(2)根据物质的化学式可以进行相关方面的计算;
(3)氧化铜和碳在高温条件下反应能生成铜和二氧化碳.
点评:本题主要考查根据物质的化学式、化学方程式计算方面的知识,书写化学方程式时要注意遵循质量守恒定律.
(2)乙醇中碳元素、氢元素、氧元素的质量比为:24:6:16=12:3:8.故填:12:3:8.
4.6g乙醇中含碳元素的质量为:4.6g×
 ×100%=2.4g.故填:2.4.
×100%=2.4g.故填:2.4.(3)最能说明这个反应已经完成的实验现象是导管口不再出现气泡.故填:导管口不再出现气泡.
碳在高温时还原氧化铜的化学方程式为:C+2CuO
 2Cu+CO2↑.
2Cu+CO2↑.解设要使80g氧化铜完全还原,需要碳的质量至少是X,
C+2CuO
 2Cu+CO2↑
2Cu+CO2↑12 160
X 80g
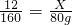
X=6g.故填:6g.
分析:(1)石油、煤、天然气属于化石燃料,核能、氢能、太阳能等属于新能源;
(2)根据物质的化学式可以进行相关方面的计算;
(3)氧化铜和碳在高温条件下反应能生成铜和二氧化碳.
点评:本题主要考查根据物质的化学式、化学方程式计算方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
 某校同学对市场上的食品疏松剂进行了如下探究.
某校同学对市场上的食品疏松剂进行了如下探究.
实验一:甲小组的同学收集到一包主要成分是小苏打(碳酸氢钠)的疏松剂
(1)取样品溶于适量的水中,测得溶液的pH大于7.
(2)向小苏打样品中滴加盐酸,有大量气泡产生,经检验该气体是二氧化碳.该反应的化学方程式为________.
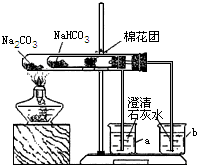
(3)同学们通过查阅资料,在老师的指导下采用了如图所示装置用小苏打和纯碱做了对比实验.实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,
b烧杯中石灰水了现白色浑浊.试回答:①在实验结束时,操作上要注意的问题是:________
②由实验(3)可以得出的结论是________.北方农村地区用“碱面”(碳酸钠)蒸馒头时,必须先将面粉发酵(产生一些有机酸)的原因是________.
实验二:乙小组的同学收集到一包名为“臭粉”的疏松剂,为探究其组成,进行实验:
(1)“臭粉”为一种白色固体,易溶于水;
(2)取少量样品与稀盐酸混合后产生了可以使石灰水变混浊的气体;
(3)取少量样品加热后,产生了有刺激性气味的气体;
(4)少量样品与氢氧化钠溶液混合后共热,产生了使湿润的红色石蕊试纸变蓝的臭气.
调查后得知,“臭粉”的主要成分是初中化学课本中一种常见的盐.
①你认为该盐是________,它加热后反应的方程式为________
②用“臭粉”作疏松剂的油炸食品放置后再销售和食用的原因可能是________.
③某些小商贩喜欢选用“臭粉”代替“小苏打”作疏松剂的原因可能是________.
实验三:丙小组同学探究小苏打、“臭粉”在制作食品过程中产生气泡的原因
(1)两种疏松剂产生的气体中都含有________.推测产生这种气体的原因有________;________.
(2)小组的同学将少许面粉加入水中取上层液体用pH试纸测得:pH=7.猜测产生气体的原因是________.
实验四:丁小组的同学在某超市发现一种复合疏松剂--发酵粉,其成分见表:
| 成分 | 所用物质 |
| 碳酸盐类 | 碳酸氢钠 |
| 酸性物质 | 柠檬酸、酒石酸等 |
| 疏松剂 | 明矾 |
| 其他成分 | 淀粉、脂肪酸等 |
(2)为测定其中碳酸氢钠的质量分数,小组的同学设计了如下实验,其主要实验步骤如下:
Ⅰ.按图组装仪器,将50.0g试样放入锥形瓶中,加入足量某酸溶液;
Ⅱ.测量一定时间内干燥管内物质增加的质量(见下列曲线);
Ⅲ.待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
Ⅳ.再次称量干燥管内物质增加的质量;
Ⅴ.重复Ⅲ和Ⅳ的操作,直至干燥管内物质质量不变.

讨论:
①步骤Ⅰ.加入样品前还应检查________,所加的酸溶液是________.
②装置乙的作用是________;从导管A处缓缓鼓入一定量的空气时,装置甲的作用是________.
③请利用有关数据计算试样中碳酸氢钠的质量分数.(写出计算过程,本小题4分)
在下表相应的空格中填上相应物质名称或化学式:
| 物质名称 | 水银 | ________ | ________ | 胆矾 |
| 化学式 | ________ | H2C03 | Ba(OH)2 | ________ |
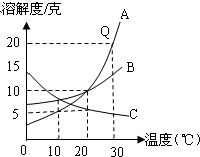 如图是A、B、C三种物质的溶解度曲线.
如图是A、B、C三种物质的溶解度曲线. 图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是
图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是