题目内容
8.在“2A+3B=2C+4D”的反应中,已知8g物质A完全反应生成11g物质C和9g物质D.若A的相对分子质量为32,则物质B的相对分子质量( )| A. | 16 | B. | 32 | C. | 48 | D. | 64 |
分析 根据质量守恒定律可以求出反应的B的质量,而后依据化学反应的物质质量之比求出B的相对分子质量即可.
解答 解:依据质量守恒定律可知反应的B的质量是:11g+9g-8g=12g,
设B的相对分子质量是x
2A+3B=2C+4D
64 3x
8g 12g
$\frac{64}{8g}$=$\frac{3x}{12g}$
x=32
故选:B.
点评 在化学方程式计算时,计算质量时与化学式前面的系数无关,在计算相对分子质量时,与化学式前面的系数是有关的,这是解题的关键.

练习册系列答案
相关题目
18.硝酸银受热时会发生如下反应:2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2X↑+O2↑.根据质量守恒定律,推测X是( )
| A. | N2O | B. | NO2 | C. | N2O5 | D. | NO |
19.下列实验操作正确的是( )
| A. | 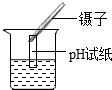 测定溶液酸碱度 测定溶液酸碱度 | B. | 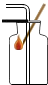 氧气验满 | C. | 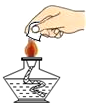 熄灭酒精灯 | D. | 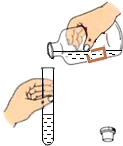 倾倒液体 |
16.头发的主要成分是蛋白质,容易受碱性溶液的侵蚀.所以我们洗发时,在用过洗发剂后再使用护发剂,这样对头发有保护作用.由此可知,护发剂的pH( )
| A. | <7 | B. | >7 | C. | =7 | D. | 比洗发剂的pH大 |
3.下列物质间不能发生复分解反应的是( )
| A. | 碳酸钠溶液和氯化钙溶液 | B. | 氢氧化钠溶液和氯化钾溶液 | ||
| C. | 碳酸钾溶液和盐酸 | D. | 硫酸铜溶液和氯化钡溶液 |
20.青少年正是长身体的时期,饮食既要均衡、适量,又要注意卫生、安全,下列说法正确的是( )
| A. | 日常饮食不要偏食 | B. | 用甲醛浸泡海鲜 | ||
| C. | 食盐加碘可防贫血 | D. | 霉变食物洗净后食用 |
6.某小组同学用盐酸和氢氧化钙进行酸和碱中和反应的探究.
(1)甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.
乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
[提出问题]甲实验后的溶液中有什么溶质?
[作出猜想]猜想一,只有CaCl2;猜想二有CaCl2和HCl;猜想三,有CaCl2和Ca(OH)2
[查阅资料]CaCl2溶液为中性.
[实验探究]为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
[实验结论]丙认为猜想二正确.
[实验评价]丙认为方案1的实验操作和方案二的设计中有不足之处,请任选其一说明其不足之处是方案1中使用pH试纸的操作不对.
大家讨论后方案3可证明猜想二正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.
[实验拓展]为节约资源和避免实验废液对环境污染,小组同学将方案1和方案3及甲实验后烧杯中剩余溶液混合(混合时未见明显现象),并对混合液中的盐分离回收,请将相关内容填入下表.
(2)请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),计算实验后所得CaCl2溶液的溶质的质量分数(写出计算过程)

(1)甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.
乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
[提出问题]甲实验后的溶液中有什么溶质?
[作出猜想]猜想一,只有CaCl2;猜想二有CaCl2和HCl;猜想三,有CaCl2和Ca(OH)2
[查阅资料]CaCl2溶液为中性.
[实验探究]为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量甲实验后的溶液于试管中) |  |  |  |
| 实验现象 | 对比标准比色卡:pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有CaCl2 |
[实验评价]丙认为方案1的实验操作和方案二的设计中有不足之处,请任选其一说明其不足之处是方案1中使用pH试纸的操作不对.
大家讨论后方案3可证明猜想二正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.
[实验拓展]为节约资源和避免实验废液对环境污染,小组同学将方案1和方案3及甲实验后烧杯中剩余溶液混合(混合时未见明显现象),并对混合液中的盐分离回收,请将相关内容填入下表.
| 要分离的盐 | 所用试剂 | 主要操作 |
| CaCl2、NaCl | Na2CO3,HCl | 混合物中加入Na2CO3溶液至不再产生沉淀,过滤,将滤液蒸发即得NaCl;将过滤后的固体加稀盐酸至不再产生气体,对溶液加热蒸发即得CaCl2 |
