题目内容
原子序数11-17元素的符号和原子结构示意图如图,请结合如图回答:
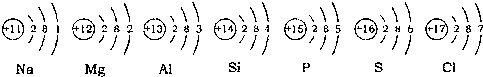
(1)以上各元素在元素周期表的第 周期.
(2)原子序数为15的原子其质子数为 ,最外层有 电子;
(3)结合如图用符号表示下列内容:
①原子序数为13的原子形成的离子符号 ,
②原子序数为12、17的元素组成化合物的化学式 .
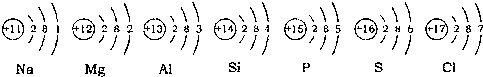
(1)以上各元素在元素周期表的第
(2)原子序数为15的原子其质子数为
(3)结合如图用符号表示下列内容:
①原子序数为13的原子形成的离子符号
②原子序数为12、17的元素组成化合物的化学式
考点:原子结构示意图与离子结构示意图,化学式的书写及意义,化学符号及其周围数字的意义
专题:化学用语和质量守恒定律
分析:(1)根据周期数等于原子核外电子层数,进行分析解答.
(2)根据原子序数=核电荷数=质子数,进行分析解答.
(3)①原子序数为13的原子为铝原子,据此进行分析解答.
②原子序数为12、17的元素分别是镁元素、氯元素,据此进行分析解答.
(2)根据原子序数=核电荷数=质子数,进行分析解答.
(3)①原子序数为13的原子为铝原子,据此进行分析解答.
②原子序数为12、17的元素分别是镁元素、氯元素,据此进行分析解答.
解答:解:(1)周期数等于原子核外电子层数,以上各元素的原子核外均有3个电子层,故在元素周期表的第3周期.
(2)原子序数=核电荷数=质子数,则原子序数为15的原子,其质子数为15;由其原子结构示意图可知,其原子核外最外层有5个电子.
(3)①原子序数为13的原子为铝原子,其原子核外最外层有3个电子,在化学反应中易失去3个电子而形成阳离子,其离子符号为:Al3+.
②原子序数为12、17的元素分别是镁元素、氯元素,镁元素显+2价,氯元素显-1价,写形成化合物的化学式为:MgCl2.
故答案为:(1)3;(2)15;5个;(3)①Al3+;②MgCl2.
(2)原子序数=核电荷数=质子数,则原子序数为15的原子,其质子数为15;由其原子结构示意图可知,其原子核外最外层有5个电子.
(3)①原子序数为13的原子为铝原子,其原子核外最外层有3个电子,在化学反应中易失去3个电子而形成阳离子,其离子符号为:Al3+.
②原子序数为12、17的元素分别是镁元素、氯元素,镁元素显+2价,氯元素显-1价,写形成化合物的化学式为:MgCl2.
故答案为:(1)3;(2)15;5个;(3)①Al3+;②MgCl2.
点评:本题难度不大,考查学生对原子结构示意图及其意义的理解,明确原子结构示意图中最外层电子数与得失电子的关系是解题的关键.

练习册系列答案
相关题目
一种闪烁晶体材料BGO(化学式为Bi4Ge3O12),其中铋(Bi)元素为+3价,则锗(Ge)元素为( )
| A、+1价 | B、+2价 |
| C、+3价 | D、+4价 |
下列叙述正确的是( )
| A、若两种粒子的核外电子数相同,这两种粒子一定是同种元素 |
| B、若两种粒子的质子数相同,这两种粒子一定是同种元素 |
| C、若两种粒子是同种元素,这两种粒子的中子数不一定相同 |
| D、若两种粒子是同种元素,这两种粒子的最外层电子数一定相同 |
下列现象或事实,用分子的相关知识加以解释,其中错误的是( )
| A、热胀冷缩,说明分子的大小随温度的改变而改变 |
| B、“酒香不怕巷子深”,说明分子在不断地运动 |
| C、5mL水和5mL酒精混合,溶液体积小于10mL,说明分子间有空隙 |
| D、水通电后生成氢气和氧气,说明在化学变化中分子可以再分 |
根据下列微粒的结构示意图判断,表示阴离子的是( )
A、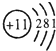 |
B、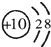 |
C、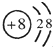 |
D、 |
水是纯净物的特征是( )
| A、是无色的 |
| B、能洗净许多物质 |
| C、由同种分子构成 |
| D、是透明的 |
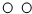 表示
表示 表示
表示 表示
表示