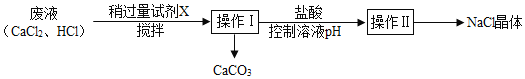
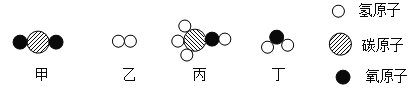
题目内容
【题目】从C、H、O、N、Ca、S、Ba、P等7种元素中选择恰当的元素,用离子符号、化学式或化学方程式按下列要求填空:
(1)两个钡离子_____;
(2)引起酸雨的大气污染物_____;
(3)配制波尔多液的碱_____;
(4)有10个电子的带电粒子_____;
(5)有氨味的固态氮肥_____;
(6)一种暗红色物质燃烧生成白烟_____;
(7)有沉淀生成的中和反应_____。
【答案】2Ba2+ SO2、NO2 Ca(OH)2 OH-或者NH4+ NH4HCO3 P ![]()
【解析】
(1)钡离子用Ba2+表示,两个钡离子表示为2Ba2+;
故填:2Ba2+。
(2)化石燃料燃烧生成的二氧化硫、二氧化氮排放到空气中,引起酸雨;
故填:SO2、NO2。
(3)农业生产上,用熟石灰和硫酸铜溶液配制波尔多液,硫酸铜是盐、熟石灰中的氢氧化钙是碱;
故填:Ca(OH)2。
(4)C原子核外有6个电子,H原子核外有1个电子、O原子核外有8个电子、N原子核外有7个电子,Ca、S、Ba、P各原子的核外电子数大于10个,核外有10个电子的带电粒子只能是C、H、O、N这四种原子中的几种原子构成的离子,所以核外有10个电子的带电粒子可能是NH4+或者OH-;
故填:NH4+。
(5)结合所学的知识,固态氮肥有:尿素[CO(NH2)2]、硫酸铵[(NH4)2SO4]、硝酸铵(NH4NO3)、碳酸氢铵(NH4HCO3),其中有氨味的是碳酸氢铵,化学式是NH4HCO3;
故填:NH4HCO3。
(6)红磷在空气中燃烧产生大量的白烟,这种暗红色物质是红磷,化学式是P;
故填:P。
(7)酸和碱作用生成盐和水的反应,叫做中和反应;酸是由氢离子和酸根离子构成的化合物;碱是由金属离子和氢氧根离子构成的化合物;所给的元素C、H、O、N、Ca、S、Ba、P中,可组成的酸是硫酸,碱是氢氧化钙或氢氧化钡,有沉淀生成的是硫酸和氢氧化钡反应生成硫酸钡沉淀和水,化学方程式是![]() ;
;
故填:![]() 。
。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案【题目】小明发现他戴的铜质眼镜架表面变绿了,经过咨询老师知道是生成了铜锈。小明和实验小组的同学决定设计并进行实验,探究铜锈的组成和铜生锈的条件。
探究1:铜锈由哪些元素组成?
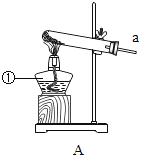
(查阅资料)铜锈受热易分解
(进行实验)利用下图所示装置对铜锈进行加热,观察到试管口有水珠生成,烧杯中澄清石灰水变浑浊,绿色固体变为黑色。
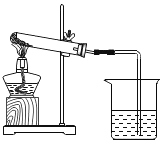
根据以上现象分析,铜锈中一定含有的元素:Cu和_____。
探究2:铜发生锈蚀的条件是什么?
(猜想与假设)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关
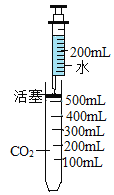
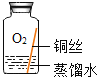
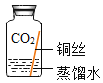
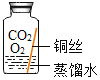
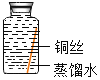
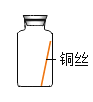
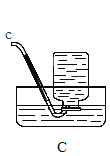
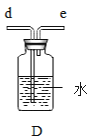
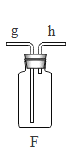
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
(1)实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是_____。
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,请在图中将实验⑤补充完整_____。
(5)由上述实验可推知,铜生锈的条件是_____。
(反思与评价)
(6)对实验进行反思后,同学们认为实验_____可以不用进行。
(7)根据实验结论,请你写出一种防止铜发生锈蚀的方法_____。