题目内容
某同学通过用碳酸钙和稀盐酸反应的实验来验证质量守恒定律.反应前小明称得碳酸钙、稀盐酸以及锥形瓶(敞口)的总质量是200g,反应结束后(碳酸钙全部反应),称得锥形瓶及里面物质的总质量变为195.6g.试计算有多少碳酸钙参加反应?该反应遵循质量守恒定律吗?请用简要的语言说明该实验应怎样改进才能达到实验目的.
解:根据题意,生成二氧化碳的质量为200g-195.6g=4.4g,
设参加反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
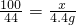 x=10g.
x=10g.
答:参加反应的碳酸钙的质量为10g.
一切化学反应均遵循质量守恒定律,该反应遵循质量守恒定律;该实验要想达到实验目的,可在锥形瓶口套一个气球,将石灰石放在气球中,稀盐酸放在锥形瓶中,使装置密封.
故答案为:10g;遵循质量守恒定律;在锥形瓶口套一个气球,将石灰石放在气球中,稀盐酸放在锥形瓶中,使装置密封.
分析:根据质量守恒定律,反应前后总质量减少的质量即为产生的二氧化碳气体的质量,再根据反应的化学方程式计算出参加反应碳酸钙的质量即可.
一切化学反应均遵循质量守恒定律;有气体参加或有气体生成的反应需在密闭容器中进行才能判断参加化学反应的反应物的总质量和生成物的总质量是否相等,上述实验总质量减少,是因为有气体生成,没有在密闭容器中进行.
点评:本题难度不是很大,考查化学方程式的计算、质量守恒定律的理解,根据质量守恒定律计算出生成二氧化碳气体的质量是解答本题的关键.
设参加反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
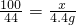 x=10g.
x=10g.答:参加反应的碳酸钙的质量为10g.
一切化学反应均遵循质量守恒定律,该反应遵循质量守恒定律;该实验要想达到实验目的,可在锥形瓶口套一个气球,将石灰石放在气球中,稀盐酸放在锥形瓶中,使装置密封.
故答案为:10g;遵循质量守恒定律;在锥形瓶口套一个气球,将石灰石放在气球中,稀盐酸放在锥形瓶中,使装置密封.
分析:根据质量守恒定律,反应前后总质量减少的质量即为产生的二氧化碳气体的质量,再根据反应的化学方程式计算出参加反应碳酸钙的质量即可.
一切化学反应均遵循质量守恒定律;有气体参加或有气体生成的反应需在密闭容器中进行才能判断参加化学反应的反应物的总质量和生成物的总质量是否相等,上述实验总质量减少,是因为有气体生成,没有在密闭容器中进行.
点评:本题难度不是很大,考查化学方程式的计算、质量守恒定律的理解,根据质量守恒定律计算出生成二氧化碳气体的质量是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
(1)分类法:利用下列4组物质请按要求填写下表横线上(填写物质的化学式或分类标准)(分类标准包括:酸、碱、盐、金属氧化物、非金属氧化物、金属单质、非金属单质)
A.ZnO、MgO、CO2、Na2O B.Cu、N2、C、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
| A | B | C | D | |
| 分类标准 | 金属氧化物 | ______ | 盐 | ______ |
| 不属于该类别的物质 | ______ | Cu | ______ | H2O |
A.通过对CO2+H2O→H2CO3 和 6CO2+6H2O
 C6H12O6+6O2两个化学反应的对比,你能得出的结论是:相同的反应物在不同的条件下______.
C6H12O6+6O2两个化学反应的对比,你能得出的结论是:相同的反应物在不同的条件下______.B.如图1所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之一:______.

(3)归纳演绎法:
某同学通过对大量化学反应前后各物质的质量总和的测定分析(如图2中的氢氧化钡溶液与硫酸钠溶液,用少量的双氧水和二氧化锰分解),得出参加化学反应的各物质的质量总和______(填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.根据该同学得出的结论可推出:高温煅烧含有杂质的石灰石125g(杂质不发生反应),充分反应后剩余固体质量为81g,则反应过程中生成二氧化碳的质量为______ g.请根据化学反应方程式列式计算①该石灰石中含碳酸钙的物质的量是多少?②该石灰石中含碳酸钙的质量分数是多少?
