题目内容
8.某工厂欲从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸锌晶体,其工业流程图如图:
(1)操作a名称是过滤;操作b名称是蒸发;操作b用到的主要仪器有铁架台、蒸发皿、玻璃棒、酒精灯等(至少写两种).
(2)图中过量A是锌;固体是铜和锌;适量B是稀硫酸;写出流程中加入适量B反应的化学方程式Zn+H2SO4═ZnSO4+H2↑.
分析 锌能和硫酸铜反应生成硫酸锌和铜;
铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气.
解答 解:(1)操作a名称是过滤;
操作b名称是蒸发;
操作b用到的主要仪器有铁架台、蒸发皿、玻璃棒、酒精灯等.
故填:过滤;蒸发;铁架台、蒸发皿、玻璃棒、酒精灯等.
(2)图中过量A是锌;
固体是铜和锌;
适量B是稀硫酸;
锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
故填:锌;铜和锌;稀硫酸;Zn+H2SO4═ZnSO4+H2↑.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
18.由于森林的过度砍伐、草场的大面积开垦,土地出现沙漠化,导致我国北方地区经常出现沙尘暴天气.请你预测当北京市出现沙尘天气时,首要污染物会是( )
| A. | 臭氧 | B. | 二氧化氮 | C. | 可吸入颗粒物 | D. | 二氧化硫 |
19.在太空舱里,为了保持舱内CO2气体含量的相对稳定,常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2.NiFe2O4中铁元素的化合价为+3价,则Ni的化合价为( )
| A. | +2 | B. | +1 | C. | +3 | D. | +4 |
16.金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.猜想1.Cr>Fe>Cu;2.Fe>Cu>Cr;3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
(1)得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 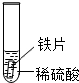 | 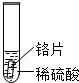 |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 无现象 |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
2.下列关于原子核的叙述中正确的是( )
①通常由中子和电子构成 ②不显电性 ③带负电荷 ④不能再分
⑤通常由质子和中子构成 ⑥体积大约相当于原子 ⑦质量大约相当于原子.
①通常由中子和电子构成 ②不显电性 ③带负电荷 ④不能再分
⑤通常由质子和中子构成 ⑥体积大约相当于原子 ⑦质量大约相当于原子.
| A. | ①⑤ | B. | ③④ | C. | ⑤⑦ | D. | ②⑥⑦ |
9.氧气是空气的主要成分之一,地球上一切生命体每时每刻都离不开氧气.
(1)根据如图所示实验,回答下列问题.
(2)根据如图所示实验,回答下列问题.
(1)根据如图所示实验,回答下列问题.
| 实验 操作 |  A.木炭在氧气中燃烧 |  B.硫在氧气中燃烧 |  C.铁丝在氧气中燃烧 |
| 实验 现象 | 发出白光,放出热量,生成使澄清石灰水变浑浊的气体. | 在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,放出热量生成有刺激性气味的气体. | 剧烈燃烧,火星四射,生成黑色固体,同时放出热量. |
| 化学方程式 | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
| 集气瓶底放少量的水,其作用是 | 吸收二氧化硫,防止二氧化硫污染空气 | 防止生成物溅落下来,炸裂瓶底 | |
| 实验 操作 |  D.镁带在空气中燃烧 |  E.测定空气中氧气的含量 |  F.甲烷在空气中燃烧 |
| 实验 现象 | 燃烧发出耀眼的白光,生成白固体,同时放热. | 燃烧放出大量的白烟 白烟,同时放热,冷却后打开止水夹,水进入集气瓶约占集气瓶体积的$\frac{1}{5}$. | 发出蓝色色火焰,罩一个干冷烧杯,烧杯内壁出现水雾,加入澄清石灰水变浑浊. |
| 化学方程式 | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
| F实验可检验甲烷的组成,此实验原理是:质量守恒定律 | |||
6.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,向滤渣中滴加稀盐酸,产生气泡,有关判断正确的是( )
| A. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| B. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| C. | 滤液中一定有银、铜和锌 | |
| D. | 滤液中一定有银和锌,可能有铜 |
7.“绿色化学”能实现零排放(即研究不排出任何废物的化学反应).密闭容器中CO和H2在一定条件下按照不同的比例可以合成不同的化工原料.根据零排放的要求,以CO和H2合成的物质不可能是( )
| A. | 乙醇(C2H6O) | B. | 甲醛(CH2O) | C. | 乙酸(C2H4O2) | D. | 甲醇(CH4O) |