题目内容
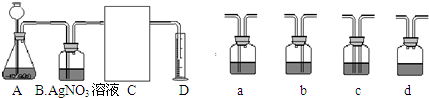
要配制l00g溶质质量分数为10%的氯化钠溶液,下列操作正确的是( )
A.将l0g氯化钠固体直接放在天平的托盘上称量
B.用100mL量筒量取90mL水时,俯视读数
C.为加快氯化钠同体的溶解,用温度计搅拌溶液
D.将配好的溶液倒入试剂瓶中,盖紧瓶塞,并贴上标签
D

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分)
a.实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过得到5g固体和111 g氯化钙溶液(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒入贴有相应标签的试剂瓶中.请回答下列问题:
(1)同学们选择的固体药品是 ;
(2)请写出题中发生反应的化学方程式 ;
(3)请根据已知条件求解生成氯化钙质量 g.
b.现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn-119,Ni-59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
试求:①合金中铜的质量分数为 .②合金中另一金属是 .
a.实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过得到5g固体和111 g氯化钙溶液(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒入贴有相应标签的试剂瓶中.请回答下列问题:
(1)同学们选择的固体药品是
(2)请写出题中发生反应的化学方程式
(3)请根据已知条件求解生成氯化钙质量
b.现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn-119,Ni-59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入酸的质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
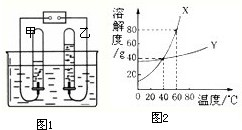 水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题: