题目内容
9.请仔细观察下面溶液的变化并回答问题.
(1)A中的试管不能(填“能”或“不能”)把水加入浓硫酸中.
(2)B中溶液变浑浊的原因是浓硫酸溶于水放热,溶液温度升高使Ca(OH)2析出
(3)A中试管内试剂改为Mg和稀盐酸,会(填“会”或“不会”)出现与上图相同的现象.
(4)ABC中Ca(OH)2溶液溶质质量分数的大小关系为A=C>B(用ABC和>、<、=表示)
分析 ①稀释浓硫酸的操作应该是酸入水,否则会使酸液飞溅发生危险.
②浓硫酸溶于水会放热,使溶液温度升高,导致氢氧化钙的溶解度变小.
③Mg和稀盐酸反应也会放热,也会出现相同的现象.
④A、B、C中A、C是常温时的氢氧化钙的饱和溶液,B是高温时的氢氧化钙的饱和溶液,利用这一关系可解决此题.
解答 解:①稀释浓硫酸的操作应该是酸入水,否则会使由于放出大量的热而使酸液飞溅发生危险.
故答案为:不能;
②浓硫酸溶于水会放热,使溶液温度升高,导致氢氧化钙的溶解度变小,溶质析出.
故答案为:浓硫酸溶于水放热,溶液温度升高使Ca(OH)2析出;
③Mg和稀盐酸反应时也会放出热量,因此会出现相同的现象.
故答案为:会;
④A、C是常温时的氢氧化钙的饱和溶液,B是温度升高后的氢氧化钙的饱和溶液,由于氢氧化钙的溶解度随温度升高而降低,故溶质质量分数的关系是A=C>B.
故答案为:A=C>B.
点评 化学实验操作的先后顺序常常影响实验的结果,对与常见的实验同学们一定要熟记实验的先后顺序;利用放热反应对氢氧化钙的溶液进行分析比较,属基础性知识考查题

练习册系列答案
相关题目
17.如表中,有关量的变化图象与其对应叙述不相符的是( )
| A. | 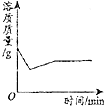 向饱和石灰水中加入少量的生石灰 向饱和石灰水中加入少量的生石灰 | |
| B. |  向一定质量含CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液 向一定质量含CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液 | |
| C. | 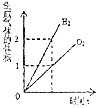 向水中加入少量稀硫酸,通电一段时间 向水中加入少量稀硫酸,通电一段时间 | |
| D. | 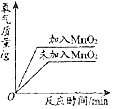 用等质量、等浓度的双氧水分别制取氧气 用等质量、等浓度的双氧水分别制取氧气 |
4.在下表中填写物质的名称,化学式及溶解性(溶、不溶、微溶)
| 名称 | 化学式 | 溶解性 | 名称 | 化学式 | 溶解性 |
| FeCl2 | 碳酸钙 | ||||
| 纯碱 | H2SO4 | ||||
| Cu(OH)2 | Na2SO4 | ||||
| 硝酸铵 | 熟石灰 |
14.下列实验操作或记录正确的是( )
| A. | 稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌 | |
| B. | 打开装有浓盐酸的试剂瓶,可看到白烟 | |
| C. | 用托盘天平称取 5.4g氯化钠 | |
| D. | 测溶液pH值时,将待测液倾倒在试纸上,将pH试纸的颜色与标准比色卡比较即可 |
1.现有①粗盐:②液态氧:③纯碱:④洁净的海水.对上述物质的分类正确的( )
| A. | 盐--------① | B. | 单质----② | C. | 碱----③ | D. | 纯净物----④ |
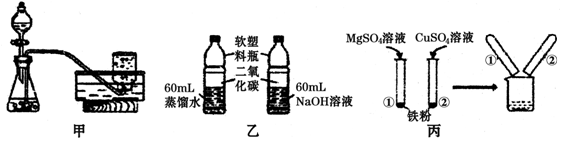
 化学兴趣小组用如图所示装置研究两个问题:
化学兴趣小组用如图所示装置研究两个问题: