题目内容
下列除去杂质的方法正确的是 ( )
选项 物质(括号内为杂质) 除去杂质的方法
A CaO(CaCO3) 加足量水溶解、过滤、洗涤、干燥
B N2(O2) 通过灼热的铜网
C CO2(H2) 在氧气中点燃
D HNO3溶液(HCl) 加过量AgNO3溶液、过滤
B
【解析】
试题分析:根据主要物质和杂质的性质的不同来分析。
A、CaO和CaCO3混合物,加入足量水后,主要物质CaO会与水反应生成氢氧化钙,错误;
B、N2和O2混合物通过灼热的铜网时,杂质氧气会与灼热的铜反应而被除去,主要物质氮气不能与之反应,故能除去杂质,正确;
C、由于CO2不可燃,也不支持燃烧,故能起到隔绝氧气的作用,所以CO2中H2不能被点燃而除去,错误;
D、HNO3和HCl混合物,加过量AgNO3溶液,杂质HCl能被反应掉,而主要物质不反应,但由于AgNO3溶液过量,故一定有剩余,则带来新杂质AgNO3溶液,错误。故选B
考点:物质除杂或净化的探究
点评:一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应,②反应时不能加入新的杂质,这是正确解题的关键。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案(本题共12分)
已知:
| 药品名称 | 熔点/℃ | 沸点(℃) | 密度g/cm3 | 溶解性 |
| 正丁醇 | -89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |
 根据题意完成下列填空:
根据题意完成下列填空:
(一)制备1-溴丁烷粗产品
在右图装置的圆底烧瓶中依次加入NaBr,10 mL正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30 min。
(1)写出制备1-溴丁烷的化学反应方程式:
__________________________________________________
(2)反应装置中加入沸石的目的是__________________。
配制体积比为1:1的硫酸所用的定量仪器为 (选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
(3)反应装置中,除了产物和水之外,还可能存在 、 等有机副产物。
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是 (选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
 (二)制备精品
(二)制备精品
将得到的粗1-溴丁烷依次用浓硫酸、水、10% 碳酸钠、水洗涤后加入无水氯化钙进行干燥,然后再将1-溴丁烷按右图装置蒸馏。
(5)收集产品时,控制的温度应在_________℃左右;
区分1-溴丁烷精品和粗品的一种方法是____________________。
(6)实验制得的1-溴丁烷的质量为10.895 g,则正丁醇的转化率为 。(保留3位小数)。

 (2012?潍坊二模)化学实验课上老师要求分组除去铁制品和锈铜币表面的锈层并对废液进行处理.请你参与并回答相关问题.
(2012?潍坊二模)化学实验课上老师要求分组除去铁制品和锈铜币表面的锈层并对废液进行处理.请你参与并回答相关问题.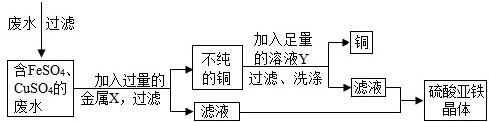
 如图是小红同学用来电解水的简易装置图.请你参与探究并回答下列问题:
如图是小红同学用来电解水的简易装置图.请你参与探究并回答下列问题: