题目内容
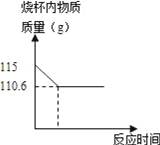
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取样品15g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应),向其中加入100g足量的稀盐酸,充分反应后烧杯内剩余物质质量变化如图所示.问:
(1)15g样品可以产生 g二氧化碳;
(2)该样品中碳酸钙的质量为多少?

【考点】根据化学反应方程式的计算.
【专题】综合计算(图像型、表格型、情景型计算题).
【分析】根据质量守恒定律,石灰石的质量与稀盐酸的质量之和减去烧杯内剩余物质的质量就是生成二氧化碳的质量;由二氧化碳的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
【解答】解:(1)由图示结合质量守恒定律可知,生成二氧化碳的质量为115g﹣110.6g=4.4g.
(2)设参加反应的碳酸钙的质量为x.
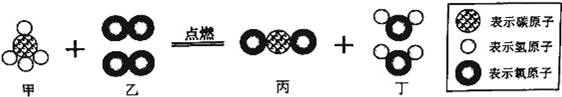
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
100 44
x 4.4g
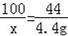
 ,
,
x=10g
石灰石中碳酸钙的质量分数为
 ×100%=67%
×100%=67%
答:(1)生成二氧化碳的质量是4.4g;(3)石灰石中碳酸钙的质量分数为67%.
【点评】本题难度不是很大,利用质量守恒定律由反应前后烧杯内物质的总质量的差计算出生成二氧化碳的质量是解答本题的突破口.

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
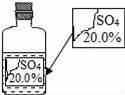
新黄冈兵法密卷系列答案一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如图所示.要求同学们进行探究,确认这瓶溶液到底是什么溶液?
【提出猜想】王老师提示:这瓶无色溶液只能是下列四种溶液中的一种:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铵溶液
【查阅资料】(1)常温下,相关物质的溶解度如下:
| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
(2)(NH4)2SO4的水溶液显酸性
【实验探究】
(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 .
(2)为确定其他几种猜想是否正确,小明同学继续进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 NaOH 溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟标准比色卡对照 | 溶液pH 小于 7 (填大于或小于或等于) | 猜想③成立 |
小雅同学认为小明实验操作②的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, 向试管中加入少量的NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口 |
| 猜想④成立,该反应的化学方程式为
|