题目内容
10.将100g石灰石放在烧杯中,加入150g稀盐酸恰好完全反应.称量剩余物的总质量为228g.求二氧化碳的质量,以及石灰石中碳酸钙的质量分数.分析 根据质量守恒定律,放出二氧化碳的质量=反应前物质质量总和-反应后物质质量总和;利用碳酸钙与盐酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出石灰石中碳酸钙的质量,然后根据质量分数公式计算即可.
解答 解:由质量守恒定律可知,放出二氧化碳的质量为:100g+150g-228g=22g;
设参与反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 22g
$\frac{100}{44}=\frac{x}{22g}$ 解之得:x=50g
石灰石中碳酸钙的质量分数为:$\frac{50g}{100g}×100%$=50%.
答:放出二氧化碳22g;石灰石中碳酸钙的质量分数为50%.
点评 本题主要考查学生利用化学方程式和质量守恒定律解答问题的能力.利用质量守恒定律,可以求出化学反应中生成气体和沉淀的质量,为进一步解题打开突破口.

练习册系列答案
相关题目
1.下列常见的物品中是用天然材料制成的是( )
| A. | 木框门 | B. | 日光灯管 | C. | 铝合金门窗 | D. | 陶瓷花瓶 |
18.物质的性质决定其用途.下列用途是利用物质物理性质的是( )
| A. | 干冰用于人工降雨 | B. | 生石灰用作食品干燥剂 | ||
| C. | 用熟石灰改良土壤的酸性 | D. | 碳酸氢钠用于治疗胃酸过多 |
9.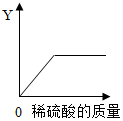 向一定量的锌粉中逐滴加入稀硫酸至过量,如图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示( )
向一定量的锌粉中逐滴加入稀硫酸至过量,如图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示( )
 向一定量的锌粉中逐滴加入稀硫酸至过量,如图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示( )
向一定量的锌粉中逐滴加入稀硫酸至过量,如图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y不可能表示( )| A. | 消耗锌粉的质量 | B. | 溶液的总质量 | ||
| C. | 生成硫酸锌的质量 | D. | 生成氢气的质量 |
6.下列过程中,不是化学变化的是( )
| A. | 铁锅生锈 | B. | 鞭炮爆炸 | C. | 石蜡熔化 | D. | 大米酿酒 |