题目内容
过氧化钠(Na2O2)因为能与水、CO2等反应产生氧气而作为供氧剂.现将39克Na2O2投入到足量的水中,发生如下反应:2Na2O2+2H2O═4NaOH+O2↑
(1)请计算生成NaOH和O2的质量.
(2)若反应开始时水的质量为69克,求反应后所得溶液的溶质的质量分数.
【答案】分析:(1)根据反应的化学方程式,由Na2O2的质量可以求出生成的NaOH和O2的质量;
(2)根据溶质质量分数的计算公式可以求出反应后所得溶液的溶质的质量分数;
解答:解:设生成NaOH的质量为x,生成O2的质量为y
2Na2O2+2H2O═4NaOH+O2↑
156 160 32
39g x y
 =
= 解得:x=40g
解得:x=40g
 =
= 解得:y=8g
解得:y=8g
据题意:溶液质量为:69g+39g-8g=100g,溶液中溶质的质量分数: ×100%=40%
×100%=40%
答:(1)生成NaOH的质量为20g,生成O2的质量为8g;
(2)反应后所得溶液的溶质的质量分数 40%.
点评:根据反应的化学方程式进行计算时,所使用的物质的质量必须为完全反应的物质的质量,未参加反应的物质质量不能代入化学方程式进行计算.
(2)根据溶质质量分数的计算公式可以求出反应后所得溶液的溶质的质量分数;
解答:解:设生成NaOH的质量为x,生成O2的质量为y
2Na2O2+2H2O═4NaOH+O2↑
156 160 32
39g x y
 =
= 解得:x=40g
解得:x=40g  =
= 解得:y=8g
解得:y=8g据题意:溶液质量为:69g+39g-8g=100g,溶液中溶质的质量分数:
 ×100%=40%
×100%=40%答:(1)生成NaOH的质量为20g,生成O2的质量为8g;
(2)反应后所得溶液的溶质的质量分数 40%.
点评:根据反应的化学方程式进行计算时,所使用的物质的质量必须为完全反应的物质的质量,未参加反应的物质质量不能代入化学方程式进行计算.

练习册系列答案
相关题目
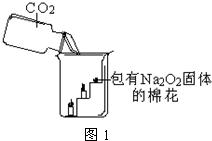


 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
