题目内容
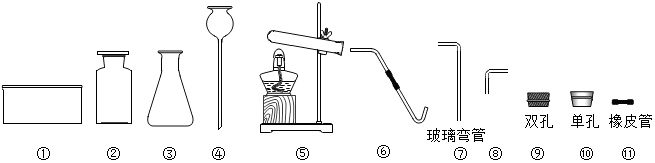
10.取用药品,如果没有说明用量就取最少量,液体取用1~2mL,固体只需盖满试管底部;读取一定量液体体积,视线应与量筒内液体的凹液面的最低处保持水平,如果俯视液面,会使读数偏大(填偏大或偏小或不变)分析 根据药品取用原则要遵循节约的原则进行分析;根据用量筒量取液体时的方法和注意事项进行分析.
解答 解:实验室取用药品应严格按照规定取用,如果没有说明用量,一般应按最少量取用,液体取1~2 mL,固体只需盖满试管底部即可;量取一定量的液体要用量筒和胶头滴管;读数时,正确的方法是视线与量筒内液体的凹液面最低处保持水平,如果俯视液面,会使读数偏大.
故答案为:最少量;1~2 mL;盖满试管底部;量筒内液体的凹液面的最低处;偏大.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.有X、Y、Z三种金属,把Y放入XSO4溶液时,溶液质量不断增加,把X放入Z (NO3)2溶液时,溶液质量不断减少,则下列符合X、Y、Z顺序排列的金属组是( )
| A. | Fe、Zn、Cu | B. | Fe、Mg、Cu | C. | Al、Fe、Ag | D. | Cu、Zn、Ag |
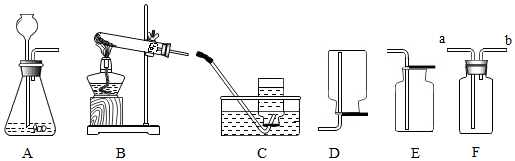
2.实验室用加热高锰酸钾的方法制取氧气,并用排水法收集,主要有以下步骤:①将药品装入试管,在试管口塞上一团棉花后,用带导管的橡皮塞塞紧试管口;②检查装置的气密性;③给试管加热;④将装置固定在铁架台上;⑤熄灭酒精灯;⑥收集气体;⑦将导管从水槽中取出.正确的操作顺序是( )
| A. | ①②④③⑥⑤⑦ | B. | ②①④③⑥⑦⑤ | C. | ②①④③⑥⑤⑦ | D. | ②①④③⑦⑥⑤ |
19.下列做法中正确的是( )
| A. | 尝药品的味道 | |
| B. | 实验剩余的药品放回原试剂瓶 | |
| C. | 加热试管里的液体时,试管口不能朝着自己或他人 | |
| D. | 加热后的试管立即用冷水冲洗 |
20. 现甲、乙两化学小组安装两套如图1所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响
现甲、乙两化学小组安装两套如图1所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响
H2O2分解速率的因素.
(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)甲小组有如表实验设计方案,完成如表.
(4)甲、乙两小组得出如图2所示数据.
①甲组实验得出的数据可知:在其他条件相同时,浓度越大,反应速率越大;,
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;因此乙组提出可以用BaO2固体与硫酸溶液反应制 H2O2,支持这一方案的理是因为在酸性条件下,过氧化氢的分解速率很慢.
 现甲、乙两化学小组安装两套如图1所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响
现甲、乙两化学小组安装两套如图1所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)MnO2催化下H2O2分解的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)甲小组有如表实验设计方案,完成如表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2溶液 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2溶液 |
①甲组实验得出的数据可知:在其他条件相同时,浓度越大,反应速率越大;,
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;因此乙组提出可以用BaO2固体与硫酸溶液反应制 H2O2,支持这一方案的理是因为在酸性条件下,过氧化氢的分解速率很慢.