题目内容
锌和稀硫酸反应生成氢气和硫酸锌.实验室里用6.77g含杂质的锌(锌不与稀硫酸反应)与49g稀硫酸恰好完全反应,制得氢气的质量为0.2g.求含杂质的锌的锌的质量分数.
设样品中锌的质量为X
Zn+H2SO4=ZnSO4+H2↑
65 2
X 0.2g
=
X=6.5g
含杂质的锌的锌的质量分数=
×100%≈96%
答:含杂质的锌的锌的质量分数为96%.
Zn+H2SO4=ZnSO4+H2↑
65 2
X 0.2g
| 65 |
| X |
| 2 |
| 0.2g |
X=6.5g
含杂质的锌的锌的质量分数=
| 6.5g |
| 6.77g |
答:含杂质的锌的锌的质量分数为96%.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
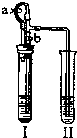 (2007?丰台区一模)某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):
(2007?丰台区一模)某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):