题目内容
下列反应都可以制取氢气,写出化学方程式:(1)水分解
(2)锌和稀硫酸反应
(3)钠和水在常温下剧烈反应制取氢气,同时生成氢氧化钠
(4)化学上利用氢化锂(LiH)和水在常温下反应制取氢气,同时生成氢氧化锂
分析:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据质量守恒定律的两个原则.
化合物中元素的化合价的代数和为零.化合物中锂常显+1价.根据化合价原则和锂的化合价可以计算出氢的化合价.
由生成氢气的质量和氢化锂与水反应的化学方程式可以计算出氢化锂的质量.
化合物中元素的化合价的代数和为零.化合物中锂常显+1价.根据化合价原则和锂的化合价可以计算出氢的化合价.
由生成氢气的质量和氢化锂与水反应的化学方程式可以计算出氢化锂的质量.
解答:解:(1)水在通电条件下反应生成氢气和氧气.
该反应的化学方程式为:2H2O
2H2↑+O2↑.
(2)锌与稀硫酸反应生成硫酸锌和氢气.
该反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑.
(3)钠与水反应生成氢氧化钠和氢气.
该反应的化学方程式为:2Na+2H2O=2NaOH+H2↑.
(4)氢化锂与水反应生成氢氧化锂和氢气.
该反应的化学方程式为:LiH+H2O=LiOH+H2↑.
设氢化锂中氢的化合价为x.
(+1)+x=0
x=-1
设需要氢化锂的质量为y.
LiH+H2O=LiOH+H2↑
8 2
x 100g
=
,x=400g
故答案为:
(1)2H2O
2H2↑+O2↑;
(2)Zn+H2SO4=ZnSO4+H2↑;
(3)2Na+2H2O=2NaOH+H2↑;
(4)LiH+H2O=LiOH+H2↑;
-1价;
需要氢化锂400g.
该反应的化学方程式为:2H2O
| ||
(2)锌与稀硫酸反应生成硫酸锌和氢气.
该反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑.
(3)钠与水反应生成氢氧化钠和氢气.
该反应的化学方程式为:2Na+2H2O=2NaOH+H2↑.
(4)氢化锂与水反应生成氢氧化锂和氢气.
该反应的化学方程式为:LiH+H2O=LiOH+H2↑.
设氢化锂中氢的化合价为x.
(+1)+x=0
x=-1
设需要氢化锂的质量为y.
LiH+H2O=LiOH+H2↑
8 2
x 100g
| 8 |
| 2 |
| x |
| 100g |
故答案为:
(1)2H2O
| ||
(2)Zn+H2SO4=ZnSO4+H2↑;
(3)2Na+2H2O=2NaOH+H2↑;
(4)LiH+H2O=LiOH+H2↑;
-1价;
需要氢化锂400g.
点评:本题主要考查化学方程式的书写、化合价的计算和化学方程式的计算,难度较大.

练习册系列答案
相关题目
甲同学对有关盐的知识进行了以下的整理.
(1)填写下表空格中的化学式:
反思:①以上盐中的金属元素的排列,可以得出是依据 顺序归纳整理的.
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液是否会具有相似的化学性质?为什么?
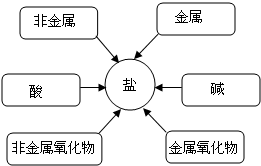
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成右图.
验证:请写出下列有盐生成的部分化学方程式:
①用稀硫酸除铁锈 ;
②盐酸和氢氧化钠反应 ;属于 反应
③古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液 ;属于 反应.
(3)甲同学在整理碳酸盐知识时,探究实验室用碳酸钙粉末、碳酸钠或碳酸氢钠,制取CO2的方法.
提出问题:实验室通常使用下列装置A制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是 .
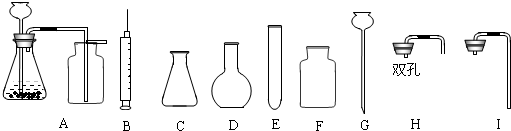
实验设计:通过控制反应物的用量来得到平稳的CO2气流的目的.因此,用碳酸盐粉末制取CO2的发生装置,可以选择 (填仪器编号)组装.
(4)向16.8g碳酸氢钠粉末中,缓缓加入100g稀盐酸,如恰好完全反应,计算生成CO2的质量和反应前稀盐酸中溶质的质量分数.(请在答卷纸上写出计算过程)
(1)填写下表空格中的化学式:
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| CaCl2 | NaCl | MgCl2 | AlCl3 |
②酸在水溶液中能解离出共同的H+,因此酸溶液具有相似的化学性质;碱在水溶液中能解离出共同的OH-,因此碱溶液也具有相似的化学性质.请据此分析上述盐溶液是否会具有相似的化学性质?为什么?
(2)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成右图.
验证:请写出下列有盐生成的部分化学方程式:

①用稀硫酸除铁锈
②盐酸和氢氧化钠反应
③古代记载的湿法冶金技术有“曾青得铁则化为铜”,其中“曾青”是指硫酸铜溶液
(3)甲同学在整理碳酸盐知识时,探究实验室用碳酸钙粉末、碳酸钠或碳酸氢钠,制取CO2的方法.
提出问题:实验室通常使用下列装置A制取二氧化碳,此装置不适合用碳酸钙粉末、碳酸钠或碳酸氢钠作反应物的原因是

实验设计:通过控制反应物的用量来得到平稳的CO2气流的目的.因此,用碳酸盐粉末制取CO2的发生装置,可以选择
(4)向16.8g碳酸氢钠粉末中,缓缓加入100g稀盐酸,如恰好完全反应,计算生成CO2的质量和反应前稀盐酸中溶质的质量分数.(请在答卷纸上写出计算过程)