题目内容
 节约是一种美德,在化学实验室中我们也能做到.某日,两组同学先后进入实验室,研究冶炼生铁的原理.
节约是一种美德,在化学实验室中我们也能做到.某日,两组同学先后进入实验室,研究冶炼生铁的原理.A组取用了一定质量的氧化铁粉末,利用如图的装置模拟生铁的冶炼,加热一段时间即结束了实验;B组为节约药品,直接利用A组剩余的药品2.4g继续进行实验,加热至完全反应后测的澄清石灰水增重0.99g.求:
(1)B组实验中参加反应的氧化铁的质量.
(2)B组取用的2.4g药品中,铁元素的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应前后澄清石灰水增重0.99克,即二氧化碳的质量是0.99g,然后根据二氧化碳的质量求氧化铁的质量,最后求铁元素的质量分数.
解答:解:反应前后澄清石灰水增重0.99克,即二氧化碳的质量是0.99g,然后根据二氧化碳的质量求氧化铁的质量,最后求氧化铁的质量分数;
设参加反应的氧化铁的质量为x
3CO+Fe2O3
2Fe+3CO2
160 132
x 0.99g
=
x=1.2g
其中铁元素的质量为1.2g×
=0.84g
2.4g药品中,铁元素的质量分数=
×100%=70%
答案:
(1)实验中参加反应的氧化铁的质量0.84g
(2)2.4g药品中,铁元素的质量分数70%
设参加反应的氧化铁的质量为x
3CO+Fe2O3
| ||
160 132
x 0.99g
| 160 |
| x |
| 132 |
| 0.99g |
x=1.2g
其中铁元素的质量为1.2g×
| 56×2 |
| 56×2+16×3 |
2.4g药品中,铁元素的质量分数=
| 0.84g |
| 1.2g |
答案:
(1)实验中参加反应的氧化铁的质量0.84g
(2)2.4g药品中,铁元素的质量分数70%
点评:本题难度不大,掌握化学方程式的计算方法和规范,注意铁元素的质量计算方法.

练习册系列答案
相关题目
最近,中国首次在珠江口钻获高纯度的“可燃冰”[主要成分是CH4?8H2O].下列关于CH4?8H2O的说法正确的是( )
| A、属于氧化物 |
| B、C、H、O原子个数比为1:20:8 |
| C、其中氢元素质量分数最高 |
| D、完全燃烧生成CO2和H2O的分子个数比为1:8 |
已知锌、镁与稀硫酸反应的化学方程式为:Mg+H2SO4=MgSO4+H2↑,Zn+H2SO4=ZnSO4+H2↑.相同质量的锌和镁分别于镁分别和足量的稀硫酸反应,产生的氢气的质量比是( )
| A、65:24 | B、24:65 |
| C、1:1 | D、无法确定 |
如图,过氧化氢在催化剂二氧化锰的作用下,迅速分解放出大量氧气.下列现象正确的是( )
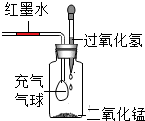

| A、气球胀大,红墨水左移 |
| B、气球缩小,红墨水左移 |
| C、气球胀大,红墨水右移 |
| D、气球缩小,红墨水右移 |
有关催化剂的说法错误的是( )
| A、反应前后本身质量不变 |
| B、反应前后化学性质不变 |
| C、可以增加生成物的质量 |
| D、可能减慢化学反应速率 |
 (1)在电解水的实验中,a、b电极相连的玻璃管上方产生的气体分别是
(1)在电解水的实验中,a、b电极相连的玻璃管上方产生的气体分别是