题目内容
将盛有等质量等质量分数的足量的稀硫酸的烧杯放在天平上、调平,同时向两烧杯中加入等质量形状相似的锌和铁.如图所示:则从开始反应到不再产生气体为止,指针偏转的情况是( )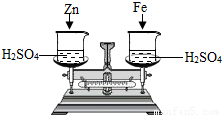
A.先偏左后偏右
B.先偏右后偏左
C.一直偏右
D.一直偏左
【答案】分析:这类题型侧重于定性分析.分析这类题目时,首先考虑的应该是反应速度,反应速度决定起始状态下,天平的偏转情况.然后考虑气体的生成量,决定最终天平的偏转情况 从而分析出天平指针偏转过程.
解答:解:由于锌的活泼性比铁强,产生氢气的速度比铁快,所以刚开始时指针应该先向右偏;
根据等质量金属完全反应放出放出氢气质量= ×金属的质量,可知铁、锌完全反应放出氢气的质量铁>锌,所以,指针应该再向左偏;
×金属的质量,可知铁、锌完全反应放出氢气的质量铁>锌,所以,指针应该再向左偏;
故选B.
点评:本题考查金属的化学性质,探讨金属与酸反应放出氢气的快慢与量的多少,属于定量计算.
解答:解:由于锌的活泼性比铁强,产生氢气的速度比铁快,所以刚开始时指针应该先向右偏;
根据等质量金属完全反应放出放出氢气质量=
 ×金属的质量,可知铁、锌完全反应放出氢气的质量铁>锌,所以,指针应该再向左偏;
×金属的质量,可知铁、锌完全反应放出氢气的质量铁>锌,所以,指针应该再向左偏;故选B.
点评:本题考查金属的化学性质,探讨金属与酸反应放出氢气的快慢与量的多少,属于定量计算.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
将盛有等质量和等质量分数的稀硫酸的两只烧杯放在托盘天平上,调节天平平衡,向右盘加入金属锌,左盘加入与锌等质量的金属镁,充分反应后,两边的酸都有剩余,则此时天平的指针指向为分度盘的( )
| A、左边 | B、右边 | C、正中 | D、无法确定 |
(2分)(2012?巴中)将盛有等质量等质量分数的足量的稀硫酸的烧杯放在天平上、调平,同时向两烧杯中加入等质量形状相似的锌和铁.如图所示:则从开始反应到不再产生气体为止,指针偏转的情况是( )
| A.先偏左后偏右 | B.先偏右后偏左 | C.一直偏右 | D.一直偏左 |
(2分)(2012?昭通)将盛有等质量、等溶质质量分数的稀硫酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铁和锌,待反应停止后(不考虑反应中水分挥发,不考虑空气成分参加反应),请判断,下列说法合理的是( )
| A.若天平仍保持平衡,烧杯中的铁一定没有剩余 |
| B.若天平失去平衡,指针一定偏向放锌的一边 |
| C.反应后两只烧杯中溶液的质量都比反应前的溶液质量减轻了 |
| D.放铁的一边产生的氢气一定比放锌的一边产生的氢气多 |
