题目内容
A、B、C、D、E是初中化学常见的物质,其中A、C是金属单质,E为非金属单质,下图是它们之间的相互转化关系.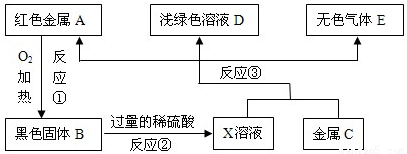
(1)反应①的基本反应类型是______反应.
(2)反应②的化学方程式为______.
(3)反应③中生成红色金属A的化学方程式为______.
(4)转化中产生无色气体E的原因是:______.
【答案】分析:根据A是红色的金属单质,所以A就是铜,铜和氧气加热会生成氧化铜,所以B就是氧化铜,氧化铜会与硫酸生成硫酸铜,所以X中有硫酸铜和硫酸,D是浅绿色的溶液,所以D中有亚铁离子,所以C就是铁,铁和硫酸铜反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,所以D就是硫酸亚铁,E就是氢气,将各物质代入转化关系中验证即可;
解答:解:(1)红色物质是铜和氧化铁,A为金属单质,则A为铜;铜在加热的条件下生成氧化铜,则B为氧化铜,该反应由两种物质生成一种物质,反应类型为化合反应.
(2)B与过量稀硫酸反应,即氧化铜与稀硫酸反应,生成硫酸铜和水,其方程式为:CuO+H2SO4=CuSO4+H2O;
(3)由硫酸铜和稀硫酸与金属C反应生成铜、浅绿色的亚铁离子的溶液和无色气体可知,金属C是铁能把Cu置换出来,其方程式为Fe+CuSO4=FeSO4+Cu
(4)由于X溶液中含有稀硫酸,而稀硫酸能与铁产生氢气,同时生成亚铁离子.
故答案为:(1)化合;(2)CuO+H2SO4=CuSO4+H2O;(3)Fe+CuSO4=FeSO4+Cu;(4)无色气体E是氢气,由金属铁与稀硫酸反应产生的,稀硫酸是过程②中加入过量导致的.
无色气体E是氢气,由金属铁与稀硫酸反应产生的,稀硫酸是过程②中加入过量导致的.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.
解答:解:(1)红色物质是铜和氧化铁,A为金属单质,则A为铜;铜在加热的条件下生成氧化铜,则B为氧化铜,该反应由两种物质生成一种物质,反应类型为化合反应.
(2)B与过量稀硫酸反应,即氧化铜与稀硫酸反应,生成硫酸铜和水,其方程式为:CuO+H2SO4=CuSO4+H2O;
(3)由硫酸铜和稀硫酸与金属C反应生成铜、浅绿色的亚铁离子的溶液和无色气体可知,金属C是铁能把Cu置换出来,其方程式为Fe+CuSO4=FeSO4+Cu
(4)由于X溶液中含有稀硫酸,而稀硫酸能与铁产生氢气,同时生成亚铁离子.
故答案为:(1)化合;(2)CuO+H2SO4=CuSO4+H2O;(3)Fe+CuSO4=FeSO4+Cu;(4)无色气体E是氢气,由金属铁与稀硫酸反应产生的,稀硫酸是过程②中加入过量导致的.
无色气体E是氢气,由金属铁与稀硫酸反应产生的,稀硫酸是过程②中加入过量导致的.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
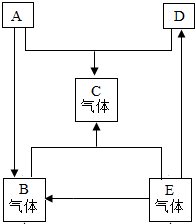 已知A、B、C、D、E是初中化学常见的五种物质,其中A、D是黑色固体,A为黑色固体单质,D为黑色固体氧化物,且其中含有人类使用最广泛的金属元素,B、C、E是无色气体,.它们在一定条件下的转化关系如下图所示(其他反应物和生成物已略去).
已知A、B、C、D、E是初中化学常见的五种物质,其中A、D是黑色固体,A为黑色固体单质,D为黑色固体氧化物,且其中含有人类使用最广泛的金属元素,B、C、E是无色气体,.它们在一定条件下的转化关系如下图所示(其他反应物和生成物已略去). 23、已知A、B、C、D、E是初中化学里常见的五种物质,它们在一定条件下能发生如图所示的转化,其中反应①是复分解反应,E是造成温室效应的主要气体.
23、已知A、B、C、D、E是初中化学里常见的五种物质,它们在一定条件下能发生如图所示的转化,其中反应①是复分解反应,E是造成温室效应的主要气体. A、B、C、D、E是常见物质,其中B和E是空气中两种气体,C是铁锈主要成分.如图所示,直线表示相互间能够反应,箭头表示转化的方向.
A、B、C、D、E是常见物质,其中B和E是空气中两种气体,C是铁锈主要成分.如图所示,直线表示相互间能够反应,箭头表示转化的方向. (2013?徐州二模)A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
(2013?徐州二模)A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题: A、B、C、D、E是初中化学中常见的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含钡元素,D、E的溶液都有颜色,
A、B、C、D、E是初中化学中常见的5种物质,它们都含有一种相同的元素,如图表示各物质之间的转化关系.其中,A为食盐的主要成分,B中含钡元素,D、E的溶液都有颜色,