题目内容
8.研究标明,饮水最好饮用白开水,小明发现家里烧开水的水壶里面有一层白色的水垢,他查资料后知道,这些水垢的主要成分是氢氧化镁、碳酸钙,且这两种物质在高温下能发生如下反应:Mg(OH)2$\frac{\underline{\;高温\;}}{\;}$MgO+H2O↑ CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
(1)上述反应属于分解反应,水壶中的水垢可以用家里厨房中的醋酸除去;
(2)设计一个实验方案,验证水垢中有Mg(OH)2、CaCO3这两种物质:
方案取少量白色固体于试管中,向其中加入足量稀盐酸,白色固体完全溶解,有气泡产生;再向上述反应后的溶液中滴加足量氢氧化钠溶液,有白色沉淀生成.
分析 (1)根据化学反应的反应物和生成物分析反应类型,依据不溶性碱、盐会与酸反应进行分析;
(2)根据碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;氯化镁能与氢氧化钠反应生成氢氧化镁沉淀进行分析.
解答 解:(1)氢氧化镁、碳酸钙这两种物质在高温下能发生的反应都是一种物质生成多种物质,属于分解反应,水壶中的水垢可以用家里厨房中的醋酸除去;
(2)由于氯化镁能与氢氧化钠反应生成氢氧化镁沉淀,溶液中又有过量的稀盐酸,所以再向上述反应后的溶液中滴加足量氢氧化钠溶液,有白色沉淀物生成,所以实验方案是:取少量白色固体于试管中,向其中加入足量稀盐酸,白色固体完全溶解,有气泡产生;再向上述反应后的溶液中滴加足量氢氧化钠溶液,有白色沉淀生成.
故答案为:(1)分解,醋酸;
(2)取少量白色固体于试管中,向其中加入足量稀盐酸,白色固体完全溶解,有气泡产生;再向上述反应后的溶液中滴加足量氢氧化钠溶液,有白色沉淀生成.
点评 本题重点考查了碳酸钙和氢氧化镁与稀盐酸反应时现象的不同,侧重酸碱盐之间化学反应的考查,熟练掌握氢氧化镁和碳酸钙能和稀盐酸反应的性质和现象不难解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18. 有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示.下列有关对苯二胺的说法 不正确的是( )
有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示.下列有关对苯二胺的说法 不正确的是( )
 有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示.下列有关对苯二胺的说法 不正确的是( )
有些年轻人喜欢染发,染发时一般要用到一种着色剂--对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示.下列有关对苯二胺的说法 不正确的是( )| A. | 对苯二胺的化学式为C6H8N2 | |
| B. | 对苯二胺能被皮肤少量吸收 | |
| C. | 对苯二胺中碳、氢、氮元素的质量分数之比为18:2:7 | |
| D. | 对苯二胺的相对分子质量(式量)为106 |
16.为防治碘缺乏病,我国正推广食用加碘盐,即在食盐中加入适量碘酸钾(KIO3),KIO3中碘元素的化合价为( )
| A. | +1 | B. | +3 | C. | +4 | D. | +5 |
13.下列关于“燃烧和灭火”的叙述正确的是( )
| A. | 煤炉生火时,用木材引燃是为了提高煤的着火点 | |
| B. | 用水可以灭火,是因为降低了可燃物的着火点 | |
| C. | 把煤做成蜂窝煤是增大煤与空气的接触面积,使煤燃烧更充分 | |
| D. | 图书馆内图书着火,立即用泡沫灭火器灭火 |
20.在一密闭的容器内有氧气、二氧化碳、水蒸气和一种未知物M,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列说法错误的是( )
| 物质 | 氧气 | M | 二氧化碳 | 水蒸气 |
| 反应前质量/g | 100 | 46 | 12 | 2 |
| 反应后质量/g | 4 | X | 100 | 56 |
| A. | 根据质量守恒定律,x的值应为0 | |
| B. | 该反应类型为置换反应 | |
| C. | 参加反应的氧气与生成的二氧化碳的质量比为12:11 | |
| D. | 物质M中含有碳、氢、氧三种元素 |
18.如图为配置50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )
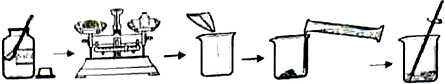

| 选项 | 操作 | 目的 |
| A | 用剩的食盐放回原试剂瓶 | 避免浪费 |
| B | 天平调平后在左、右托盘中各垫一张相同的纸 | 保证称取的食盐质量更准确 |
| C | 用50ml量筒替代天平量取所需的水 | 更加简便 |
| A. | A | B. | B | C. | C |
