题目内容
根据化学式:SO2、SO3计算:
(1)SO3的相对分子质量
(2)SO2中氧元素的质量分数
(3)100克二氧化硫中含硫元素的质量为多少克?
(4)多少克三氧化硫中含氧元素4.8克?
(5)160克三氧化硫和多少克二氧化硫含氧元素的质量相等?
(1)SO3的相对分子质量
(2)SO2中氧元素的质量分数
(3)100克二氧化硫中含硫元素的质量为多少克?
(4)多少克三氧化硫中含氧元素4.8克?
(5)160克三氧化硫和多少克二氧化硫含氧元素的质量相等?
考点:相对分子质量的概念及其计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量的计算方法来解答;
(2)由元素的质量分数的计算方法计算即可;
(3)根据元素的质量=化合物的质量×化合物中该元素的质量分数来解答;
(4)根据化合物的质量=元素的质量÷化合物中该元素的质量分数来解答;
(5)由160g三氧化硫中氧元素的质量和SO2中氧元素的质量分数可以计算出SO2的质量.
(2)由元素的质量分数的计算方法计算即可;
(3)根据元素的质量=化合物的质量×化合物中该元素的质量分数来解答;
(4)根据化合物的质量=元素的质量÷化合物中该元素的质量分数来解答;
(5)由160g三氧化硫中氧元素的质量和SO2中氧元素的质量分数可以计算出SO2的质量.
解答:解:(1)SO3的相对分子质量=32+(16×3)=80;
(2)SO2中氧元素的质量分数=
×100%=
×100%=50%;
(3)100克二氧化硫中含硫元素的质量为:100g×50%=50g;
(4)含氧元素4.8克,需要三氧化硫的质量为:
=8g;
(5)设二氧化硫的质量为x,则
160g×
×100%=x×50%,解得:x=192g.
故答案为:(1)80;(2)50%;(3)50g;(4)8g;(5)192g.
(2)SO2中氧元素的质量分数=
| 氧的相对原子质量×氧原子个数 |
| 二氧化硫的相对分子质量 |
| 16×2 |
| 32+16×2 |
(3)100克二氧化硫中含硫元素的质量为:100g×50%=50g;
(4)含氧元素4.8克,需要三氧化硫的质量为:
| 4.8g | ||
|
(5)设二氧化硫的质量为x,则
160g×
| 16×3 |
| 16×3+32 |
故答案为:(1)80;(2)50%;(3)50g;(4)8g;(5)192g.
点评:本题难度不大,考查利用化学式的有关计算,属于基础性考查题.

练习册系列答案
相关题目
下列关于溶液的说法正确的是( )
| A、溶液一定是无色透明的混合物 |
| B、饱和溶液一定是浓溶液 |
| C、溶液加水稀释前后溶质的质量不变 |
| D、碘酒中的溶剂是碘 |
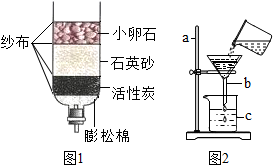 化学课外兴趣小组活动,同学们取了一定量的水做水样,请根据下列实验回答问题.
化学课外兴趣小组活动,同学们取了一定量的水做水样,请根据下列实验回答问题.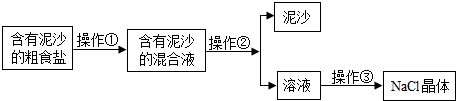
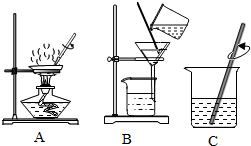
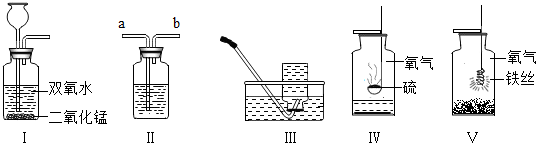

 某同学对含有泥沙和碳酸钠的粗盐进行提纯并配制一定质量分数的NaCl溶液,请回答:
某同学对含有泥沙和碳酸钠的粗盐进行提纯并配制一定质量分数的NaCl溶液,请回答: