题目内容
工业上用电解水的方法制高纯度的氧气,该反应的化学方程式 ,该反应的基本反应类型 ;该反应中在阳极产生的气体是 ,阴极和阳极产生的气体体积比为 ,H2O、H2 和O2物质的量之比为 ;生成的氢气可与氧化铜反应,该反应的现象是 ,写出该反应的化学方程式 ,该反应中还原剂是 .
【答案】分析:电解水实验阴极产生氢气,阳极产生氧气且二者体积比为2:1;氢气还原氧化铜生成铜和水.得到氧被氧化还原剂.
解答:解:电解水生成氧气和氢气,该反应的化学方程式为2H2O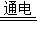 2H2↑+O2↑,该反应的反应物为一种,生成物为两种,属于分解反应;该反应中在阳极产生的气体是氧气,阴极产生氢气,用氢气与氧气的体积比为2:1,所以阴极和阳极产生的气体体积比为 2:1,H2O、H2 和O2物质的量之比为 2:2:1;生成的氢气可与氧化铜反应生成铜和水,该反应的现象是 生成红色物质,试管口有水珠生成,该反应的化学方程式H2+CuO
2H2↑+O2↑,该反应的反应物为一种,生成物为两种,属于分解反应;该反应中在阳极产生的气体是氧气,阴极产生氢气,用氢气与氧气的体积比为2:1,所以阴极和阳极产生的气体体积比为 2:1,H2O、H2 和O2物质的量之比为 2:2:1;生成的氢气可与氧化铜反应生成铜和水,该反应的现象是 生成红色物质,试管口有水珠生成,该反应的化学方程式H2+CuO 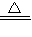 Cu+H2O,该反应中氢气夺取氧化铜中的氧,是还原剂.
Cu+H2O,该反应中氢气夺取氧化铜中的氧,是还原剂.
故答案为,2H2O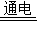 2H2↑+O2↑,分解; 氧气(或O2 ),2:1,为 2:2:1; 生成红色物质,试管口有水珠生成,H2+CuO
2H2↑+O2↑,分解; 氧气(或O2 ),2:1,为 2:2:1; 生成红色物质,试管口有水珠生成,H2+CuO 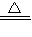 Cu+H2O,氢气( H2 ).
Cu+H2O,氢气( H2 ).
点评:明确电解水的原理、现象、氢气还原氧化铜的原理、现象以及氧化剂还原剂的判断是解答本题关健.
解答:解:电解水生成氧气和氢气,该反应的化学方程式为2H2O
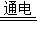 2H2↑+O2↑,该反应的反应物为一种,生成物为两种,属于分解反应;该反应中在阳极产生的气体是氧气,阴极产生氢气,用氢气与氧气的体积比为2:1,所以阴极和阳极产生的气体体积比为 2:1,H2O、H2 和O2物质的量之比为 2:2:1;生成的氢气可与氧化铜反应生成铜和水,该反应的现象是 生成红色物质,试管口有水珠生成,该反应的化学方程式H2+CuO
2H2↑+O2↑,该反应的反应物为一种,生成物为两种,属于分解反应;该反应中在阳极产生的气体是氧气,阴极产生氢气,用氢气与氧气的体积比为2:1,所以阴极和阳极产生的气体体积比为 2:1,H2O、H2 和O2物质的量之比为 2:2:1;生成的氢气可与氧化铜反应生成铜和水,该反应的现象是 生成红色物质,试管口有水珠生成,该反应的化学方程式H2+CuO 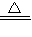 Cu+H2O,该反应中氢气夺取氧化铜中的氧,是还原剂.
Cu+H2O,该反应中氢气夺取氧化铜中的氧,是还原剂.故答案为,2H2O
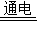 2H2↑+O2↑,分解; 氧气(或O2 ),2:1,为 2:2:1; 生成红色物质,试管口有水珠生成,H2+CuO
2H2↑+O2↑,分解; 氧气(或O2 ),2:1,为 2:2:1; 生成红色物质,试管口有水珠生成,H2+CuO 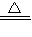 Cu+H2O,氢气( H2 ).
Cu+H2O,氢气( H2 ).点评:明确电解水的原理、现象、氢气还原氧化铜的原理、现象以及氧化剂还原剂的判断是解答本题关健.

练习册系列答案
相关题目