题目内容
(1)指出本实验的两处错误:①______; ②______.
(2)本实验进行的是______操作,目的是除去水中的______.
【答案】分析:过滤是把不溶于液体的固体与液体分离的一种方法,过滤液体时,注意“一贴、二低、三靠”的原则;据此进行分析解答.
解答:解:(1)过滤液体时,注意“一贴、二低、三靠”的原则,图中没有用玻璃棒引流,漏斗下端没有紧靠在烧杯内壁上.
(2)图中进行的实验是过滤操作,过滤是把不溶于液体的固体与液体分离的一种方法,故进行该实验的目的是除去水中的难溶于水的杂质.
故答案为:(1)①没有用玻璃棒引流;②漏斗下端没有紧靠在烧杯内壁上;
(2)过滤;难溶于水的杂质.
点评:本题难度不大,掌握过滤操作的原理、注意事项(“一贴、二低、三靠”)等是正确解答本题的关键.
解答:解:(1)过滤液体时,注意“一贴、二低、三靠”的原则,图中没有用玻璃棒引流,漏斗下端没有紧靠在烧杯内壁上.
(2)图中进行的实验是过滤操作,过滤是把不溶于液体的固体与液体分离的一种方法,故进行该实验的目的是除去水中的难溶于水的杂质.
故答案为:(1)①没有用玻璃棒引流;②漏斗下端没有紧靠在烧杯内壁上;
(2)过滤;难溶于水的杂质.
点评:本题难度不大,掌握过滤操作的原理、注意事项(“一贴、二低、三靠”)等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下载:
某化学兴趣小组有一次活动的内容是:对一包铁矿石粉末的组成进行探究,请你参与并回答有关问题.
[教师提醒]它由菱铁矿(FeCO3)、赤铁矿(Fe2O3)、磁铁矿(Fe3O4)三种固体粉末中的一种或两种组成.
[提出猜想]试样粉末主要成分可能有:①只是FeCO3、②只是Fe2O3、③只是Fe3O4、④FeCO3和Fe2O3、⑤FeCO3和Fe3O4、⑥Fe2O3和Fe3O4.
[查阅资料](1)FeCO3受热易分解FeCO3 FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,
FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,
(2)铁矿石粉末中的杂质不参加反应.
[探究思路]先利用物质的性质不同设计实验探究其成分,然后再选择适当的试剂和方法通过实验测定其含量.(装置内空气中的水蒸气、CO2忽略不计)
[实验探究]
(1)取适量试样粉末装入试管中,加入适量的盐酸,没有气泡产生,从而排除猜想中的________(填猜想中的序号).
(2)为进一步确定试样粉末的组成,称取该粉末10.0g装入硬质玻璃管中,在通风厨按如图进行实验.

开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 | |
| a管 | 玻璃管和试样粉末的总质量为70.0g | 玻璃管和固体物质的总质量为67.6g |
| b瓶 | 洗气瓶和所盛溶液的总质量为200.0g | 洗气瓶和瓶中物质的总质量为206.6g |
(3)为了防止溶液倒吸,本实验最后停止加热前是否需要先断开装置中a和b的连接处?________(填需要或不需要),理由是________.
(4)b装置中可能会发生多个化学反应,任写出其中1个反应的化学方程式:________.
[反思评价]
(5)本实验的尾气是否需处理?如需处理,请回答如何处理,如不需处理,请说明理由:________.
(6)通过计算确定,该铁矿石试样的主要成分,指出哪个猜想是正确的(已知铁矿石的纯度为80.0%).
解:
 (1)指出本实验的两处错误:
(1)指出本实验的两处错误: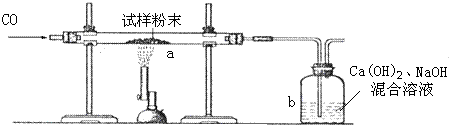
 (1)指出本实验的两处错误:
(1)指出本实验的两处错误: