题目内容
刘玮同学根据所学的化学知识,利用家庭现有器材自行设计了一个简易净水器,并成功地将一瓶墨水进行了净化.

(1)刘玮设计的净水器利用的化学原理是________.
(2)如果让你设计一个简易净水器,你的实验方案是(可用实物示意图表示):________________________.
解析:
|
解答:(1)活性炭的吸附作用(2)在可渗透的容器(如漏斗、带塞的硬质玻璃管、底部钻有小孔的塑料杯等)的底部铺上适量的棉花,再在上面铺上足量的活性炭,即可作为简易净水器.也可用如图表示. 名师导引:红墨水是可溶性杂质,可用木炭或活性炭吸附墨水中的色素. |

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡。为了解其反应过程,他与学习小组的同学进行了如下探究。
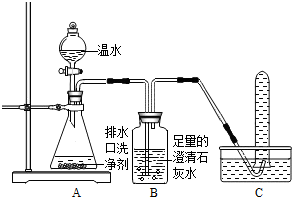
【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验。

A B C
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺。由此同学们得出结论:生成的两种气体分别是: (填化学式)。B中有关反应的化学方程式是 。
【探究二】
(1)实验过程:
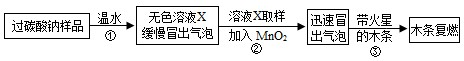
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
 |
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设: 根据以上实验现象,X溶液中一定存在的溶质是 ;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种。
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3 + CaCl2 ═ CaCO3↓ + 2NaCl。
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同。
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验。请将下列实验方案填写完整。
| 实验操作 | 主要实验现象 | 结论 |
| ① | 证明溶液中有Na2CO3 | |
| ② | 证明溶液中无NaHCO3 | |
| ③ | 证明溶液中无NaOH |
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀。于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生 (写方程式)这样的反应?于是,同学们进行了新的探究实验。
 (2013?潍城区二模)小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
(2013?潍城区二模)小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.