题目内容
6.下列关于空气的说法正确的是( )| A. | 空气中氧气的质量分数是21% | |
| B. | CO2是空气中除氮气和氧气之外含量最多的气体 | |
| C. | 分离液态空气时,首先分离出来的是氧气 | |
| D. | 分离液态空气制造氧气是利用空气中各成分的沸点不同进行的 |
分析 根据空气中各成分的体积分数:按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%;根据分离液态空气制取氧气的原理,进行分析判断即可.
解答 解:A、空气中氧气的体积分数(而不是质量分数)是21%,故选项说法错误.
B、稀有气体是空气中除氮气和氧气之外含量最多的气体,故选项说法错误.
C、分离液态空气法制取氧气的原理是在低温条件下加压,使空气转变为液态空气,然后蒸发;由于液态氮的沸点比液态氧的沸点低,因此氮气首先从液态空气中蒸发出来,剩下的主要是液态氧,故选项说法错误.
D、分离液态空气法制取氧气的原理是在低温条件下加压,使空气转变为液态空气,然后蒸发,利用的是空气中各成分的沸点不同进行的,故选项说法正确.
故选:D.
点评 本题难度不大,掌握空气的组成成分、分离液态空气制取氧气的原理是正确解答本题的关键.

练习册系列答案
相关题目
19.下列属于分解反应的是( )
| A. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | |
| B. | 石灰石+盐酸→氯化钙+二氧化碳+水 | |
| C. | 氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气 | |
| D. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
17.下列对有关物质的性质及其相关用途的叙述正确的是( )
①氧气易溶于水,使得鱼能在水中生存.
②氮气不燃烧也不支持燃烧,难溶于水.
③氧气能支持燃烧,所以可以做火箭的高能燃料.
④氧气能与许多物质发生氧化反应.
①氧气易溶于水,使得鱼能在水中生存.
②氮气不燃烧也不支持燃烧,难溶于水.
③氧气能支持燃烧,所以可以做火箭的高能燃料.
④氧气能与许多物质发生氧化反应.
| A. | ②④ | B. | ①③ | C. | ①②③ | D. | ①②④ |
14.为研究锌和铝的金属活动性,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出铝与盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有Al2O3(填化学式),
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;氯化铝为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝;
假设b:该灰黑色沉淀可能含有氯化铝和铝;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
【得出结论】由实验①可判断假设c不成立,再集合②和③可得出假设b成立.
(4)若①中小明的实验能比较锌和铝的金属活动性强弱,其所依据的现象是产生气泡的速率,从操作可行性的角度,你认为比较难以控制铝片和锌粒的表面积相同; 从设计方法的角度,你认为还需要控制金属的纯度,盐酸的浓度等变量.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出铝与盐酸反应的化学方程式:2Al+6HCl═2AlCl3+3H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是未去膜的铝片表面有Al2O3(填化学式),
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;氯化铝为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝;
假设b:该灰黑色沉淀可能含有氯化铝和铝;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如下实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(4)若①中小明的实验能比较锌和铝的金属活动性强弱,其所依据的现象是产生气泡的速率,从操作可行性的角度,你认为比较难以控制铝片和锌粒的表面积相同; 从设计方法的角度,你认为还需要控制金属的纯度,盐酸的浓度等变量.
1.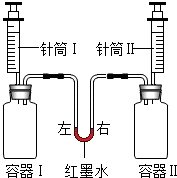 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
(1)实验a中,容器Ⅰ内产生的现象是澄清石灰水变浑浊.
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
 如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.
如图所示进行实验,同时将针筒内全部液体迅速注入容器中.实验内容如下表所示.实验开始前红墨水左右两端液面保持相平,容器Ⅰ、Ⅱ体积相同,装置气密性良好.
| 实验 编号 | 容器I | 针筒I | 容器Ⅱ | 针筒Ⅱ | 红墨水 液面位置 |
| a | 10mL 水 | NaCl | 10mL 水 | 保持 左高右低 | |
| b | 二氧化碳 (充满) | 10mL 澄清石灰水 | 二氧化碳 (充满) | 10mlL浓氢氧化钠溶液 | |
| c | 1g锌 | 15mL盐酸 | 1g镁 | 15mL盐酸 |
红墨水液面位置发生变化的原因是Ca(OH)2+CO2═CaCO3↓+H2O (用化学方程式表示).
(2)实验b中,针筒Ⅰ、Ⅱ内盐酸足量且溶质质量分数相同,产生气泡更剧烈的是容器Ⅱ (填“Ⅰ”或“Ⅱ”).红墨水液面位置变化情况是先是左高右低,最终红墨水左右两端液面保持相平.反应结束并恢复到原来的温度后,两边的红墨水保持相平.
11.下列有关燃烧和爆炸的说法错误的是( )
| A. | 燃烧一定发光、发热 | |
| B. | 爆炸也可能因物理变化引起 | |
| C. | 燃烧一定是化学变化 | |
| D. | 氢气与空气混合点燃一定会发生爆炸 |
 二氧化碳若合理利用,是一种重要的原料.
二氧化碳若合理利用,是一种重要的原料.
