题目内容
6.下表是某些食物的近似PH值,下列说法中正确的是( )| 柠檬 | 鸡蛋清 | 苹果 | 西红柿 | 牛奶 |
| 2.3 | 7.9 | 3.1 | 4.2 | 6.5 |
| A. | 牛奶和鸡蛋清属碱性食品 | B. | 胃酸过多的人应少吃苹果 | ||
| C. | 柠檬汁能使酚酞变红色 | D. | 西红柿的酸性比苹果强 |
分析 酸性溶液的pH小于7,且酸性越强,pH越小;碱性溶液的pH大于7,碱性越强,pH越大;牛奶显酸性,鸡蛋清显碱性;胃酸过多的人应少吃显酸性的食物;酚酞试液遇酸性溶液不变色;当溶液的PH<7时,随着PH的减小酸性增强;
解答 解:A、牛奶显酸性,鸡蛋清显碱性.故选项错误.
B、苹果显酸性,胃酸过多的人应少吃苹果.故选项正确;
C、柠檬汁显酸性,不能使酚酞试液变色.故选项错误;
D、苹果pH-3.1,西红柿pH=4.2,西红柿的酸性比苹果酸性弱.故选项错误;
故选B
点评 解答本题要掌握溶液的酸碱性和溶液PH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论

练习册系列答案
相关题目
3.如图为元素周期的一部分,下列说法错误的是( )


| A. | 碳元素只能形成一种单质 | B. | 氢是非金属元素 | ||
| C. | 氧的相对原子质量为16.00 | D. | C、N、O的原子序数依次增加 |
1.下列粒子中,决定元素化学性质的是( )
| A. | 质子数 | B. | 最外层电子数 | C. | 电子数 | D. | 中子数 |
11.除去下列各组物质中的少量杂质,所用方法正确的是A
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸 |
18.元素在自然界里分布并不均匀,地壳中含量的多少分析,最丰富的金属元素是( )
| A. | Fe | B. | Al | C. | O | D. | Si |
15.有四种微粒的结构示意图如下:

关于它们的下列说法错误的是( )

关于它们的下列说法错误的是( )
| A. | 乙表示的微粒是一种阴离子 | |
| B. | 甲和丁是同种元素的不同微粒 | |
| C. | 上述微粒中有两种属于非金属元素 | |
| D. | 乙和丙最外层电子数目相同,化学性质相似 |
9.在化学王国里,数字被赋予了丰富的内涵.对于①2H、②2NH3、③SO2、④Mg2+、⑤2MnO4-、⑥H2O,关于这些化学用语中数字“2”的说法正确的是( )
| A. | 表示分子中原子个数的是③⑥ | B. | 表示离子所带电荷数的是④⑤ | ||
| C. | 表示离子个数的是④⑤ | D. | 表示分子个数的是①② |
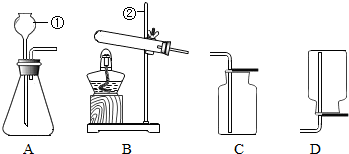 现有如图初中化学常用的制取气体部分装置.请完成以下各题:
现有如图初中化学常用的制取气体部分装置.请完成以下各题: