题目内容
13. 某饮用矿泉水1000g中的成分如图所示.
某饮用矿泉水1000g中的成分如图所示.(1)此矿泉水中至少含有七种元素.
(2)一个偏硅酸分子中一共含有6个原子.
(3)偏硅酸的相对分子质量为78.
(4)在偏硅酸H2SiO3中,氢元素与氧元素的质量比为1:24(填最简整数比).
(5)在偏硅酸H2SiO3中,求算硅元素的质量分数为35.9%(精确到0.1%).
(6)某同学喝了500g该矿泉水,他同时摄入的硅元素的质量为2.5mg.
分析 (1)根据饮用矿泉水中的成分表,进行分析解答.
(2)根据化学式的含义分析;
(3)根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(4)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(4)根据某1000g饮用矿泉水中含有钾5mg,进行分析解答.
解答 解:(1)由饮用矿泉水中的成分表,此矿泉水中至少含有氢、硅、氧、钾、钠、钙、镁七种元素.
(2)一个偏硅酸分子由2个氢原子,1个硅原子,3个氧原子,一共6个原子.
(3)偏硅酸的相对分子质量为1×2+28+16×3=78,
(4)偏硅酸中氢元素与氧元素的质量比为(1×2):(16×3)=1:24.
(5)硅元素的质量分数的计算式为$\frac{28}{78}$×100%=35.9%.
(4)某1000g饮用矿泉水中含有钾5mg,则某同学喝了500g该矿泉水,他同时摄入的钾元素的质量为5mg×$\frac{500mg}{1000mg}$=2.5mg.
故答案为:(1)七;(2)6;(3)78;(4)1:24;(3)35.9%;(4)2.5.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3. 如图是某反应前后的微观示意图,下列说法正确的是( )
如图是某反应前后的微观示意图,下列说法正确的是( )
 如图是某反应前后的微观示意图,下列说法正确的是( )
如图是某反应前后的微观示意图,下列说法正确的是( )| A. | 反应中有单质生成 | B. | 是化合反应 | ||
| C. | 反应前后分子种类不变 | D. | 参加反应的两种分子个数比为4:1 |
4.空气中含量较多化学性质比较活泼的气体是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
1.下列现象不能用质量守恒定律解释的是( )
| A. | 蜡烛燃烧时慢慢变短 | B. | 澄清石灰水露置在空气中变重 | ||
| C. | 镁带燃烧时,生成物的质量会增加 | D. | 100g干冰完全汽化成100g气体 |
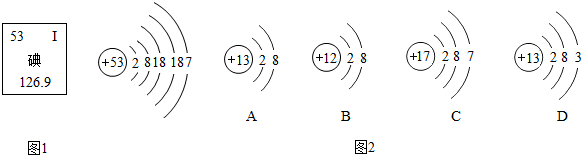
3.对于具有相同质子数的粒子,下列叙述正确的是( )
| A. | 一定是同种元素 | B. | 一定是由同种元素组成的粒子 | ||
| C. | 一定具有相同的电子数 | D. | 可能是单质,也可能是化合物 |
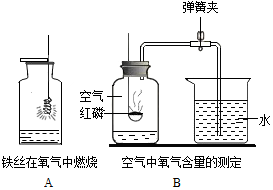 下列是初中化学常见的两个实验,回答下列问题:
下列是初中化学常见的两个实验,回答下列问题: