题目内容
某同学分别做了如下三个实验,所得数据如下表:
(1)在三次实验中第 次恰好完全反应,第 次实验中氢气有剩余,剩余 g;
(2)第 次实验中氧气有剩余,剩余 g;
(3)这三次实验 (填“是”或“不是”)都符合质量守恒定律.
| 物质的质量 | 第一次 | 第二次 | 第三次 |
| 反应前氢气的质量/g | 2 | 2 | 2 |
| 反应前氧气的质量/g | 12 | 16 | 20 |
| 反应后生成水的质量/g | 13.5 | 18 | 18 |
(2)第
(3)这三次实验
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:氢气燃烧生成水,根据反应的化学方程式可以判断反应物、生成物之间的质量比,进一步可以判断第几次恰好完全反应、那次实验中哪种物质有剩余.
解答:解:氢气燃烧的化学方程式及其反应物、生成物之间的质量比为:2H2+O2
2H2O,
4 32 36
(1)当反应物氢气和氧气的质量比是4:32=1:8,第2次实验中,氢气和氧气的质量比是2:16=1:8,恰好完全反应.
设12g氧气和氢气恰好反应时,氢气的质量为x,
2H2+O2
2H2O,
4 32
x 12g
=
x=1.5g
第1次实验中,氢气过量,剩余氢气的质量为:2g-1.5g=0.5g,
(2)根据反应的化学方程式可知,32g氧气和4g氢气恰好完全反应,2g氢气和16g氧气恰好完全反应,第3次实验中,氧气过量,剩余氧气的质量为:20g-16g=4g;
(3)这三次实验都符合质量守恒定律.
答案:
(1)2 1 0.5
(2)3 4
(3)是
| ||
4 32 36
(1)当反应物氢气和氧气的质量比是4:32=1:8,第2次实验中,氢气和氧气的质量比是2:16=1:8,恰好完全反应.
设12g氧气和氢气恰好反应时,氢气的质量为x,
2H2+O2
| ||
4 32
x 12g
| 4 |
| x |
| 32 |
| 12g |
x=1.5g
第1次实验中,氢气过量,剩余氢气的质量为:2g-1.5g=0.5g,
(2)根据反应的化学方程式可知,32g氧气和4g氢气恰好完全反应,2g氢气和16g氧气恰好完全反应,第3次实验中,氧气过量,剩余氧气的质量为:20g-16g=4g;
(3)这三次实验都符合质量守恒定律.
答案:
(1)2 1 0.5
(2)3 4
(3)是
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
对下列事实解释不正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 体温计中的水银(汞)热胀冷缩 | 原子间间隔改变 |
| B | 一滴水中大约有1.67×1021个水分子 | 分子很小 |
| C | 敞口容器中的酒精逐渐减少 | 分子是不断运动的 |
| D | 炎热的夏天自行车车胎容易爆裂 | 夏天温度高,分子变大 |
| A、A | B、B | C、C | D、D |
下列没有发生化学变化的是( )
A、 绿色植物光合作用 |
B、 氮气充入食品包装 |
C、 用纯碱蒸制馒头 |
D、 铁锅生锈 |
下列四组物质中,前者属纯净物,后者属混合物的是( )
| A、液态氮、冰水混合物 |
| B、液态氧、石灰水 |
| C、水、高锰酸钾 |
| D、空气、加热高锰酸钾制取氧气后剩余的固体 |
下列物质中属于纯净物的是( )
| A、冰水混合物 | B、硬水 |
| C、人呼出的气体 | D、净化后的空气 |
收集一瓶氢气应采用的方法是( )
| A、向上排气法 | B、排水法 |
| C、排气法 |

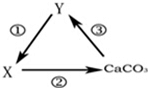 如图表示的是中学化学中常见的物质间的转化关系.请写出写出第②步对应转化关系的化学方程式
如图表示的是中学化学中常见的物质间的转化关系.请写出写出第②步对应转化关系的化学方程式