题目内容
现有一包由氧化铜、氢氧化铜、碳酸铜组成的混合物5g,向其中加入50g溶质质量分数为9.8%的稀硫酸恰好完全反应,则反应后所得溶液中的溶质质量为( )A.6.5g
B.8.2g
C.8g
D.10g
【答案】分析:根据已有的知识进行,氧化铜、氢氧化铜和碳酸铜与硫酸反应生成硫酸铜,根据硫酸的质量即可求出生成硫酸铜的质量.
解答:解:CuO+H2SO4=CuSO4+H2O,
Cu(OH)2+H2SO4=CuSO4+2H2O,
CuCO3+H2SO4=CuSO4+H2O+CO2↑,可以看出,硫酸和生成硫酸铜之间的质量关系为:H2SO4----CuSO4,设生成的硫酸铜的质量为x
H2SO4----CuSO4
98 160
50g×9.8% x
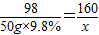 x=8g
x=8g
观察选项,故选C.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式结合题干提供的数据进行.
解答:解:CuO+H2SO4=CuSO4+H2O,
Cu(OH)2+H2SO4=CuSO4+2H2O,
CuCO3+H2SO4=CuSO4+H2O+CO2↑,可以看出,硫酸和生成硫酸铜之间的质量关系为:H2SO4----CuSO4,设生成的硫酸铜的质量为x
H2SO4----CuSO4
98 160
50g×9.8% x
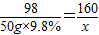 x=8g
x=8g观察选项,故选C.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式结合题干提供的数据进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
现有一包由氧化铜、氢氧化铜、碳酸铜组成的混合物5g,向其中加入50g溶质质量分数为9.8%的稀硫酸恰好完全反应,则反应后所得溶液中的溶质质量为( )
| A、6.5g | B、8g | C、8.2g | D、10g |