题目内容
将6.2克氧化钠粉末投入43.8克水中,完全溶解后,计算所得溶液中溶质的质量分数.
解:溶解后溶质是NaOH,设生成NaOH的质量为x;
Na2O+H2O=2NaOH
62 40×2
6.2g x
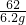 =
=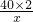 ,
,
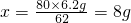 ;
;
则NaOH的质量分数=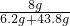 ×100%=16%;
×100%=16%;
答:所得溶液中溶质的质量分数是16%.
分析:由于氧化钠能够和水发生化学反应,因此所得溶液中的溶质是生成的氢氧化钠,由于在反应的过程中并没有沉淀和气体生成,因此溶液的质量则为氧化钠和水的质量总和;最后根据溶质质量分数=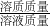 ×100%即可求得所得溶液中溶质的质量分数.
×100%即可求得所得溶液中溶质的质量分数.
点评:本题难度较大,主要考查了有关化学方程式的溶液中溶质的质量分数的计算,培养学生的综合应用能力;关键是要知道溶液的溶质是谁.
Na2O+H2O=2NaOH
62 40×2
6.2g x
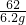 =
=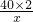 ,
,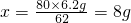 ;
;则NaOH的质量分数=
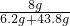 ×100%=16%;
×100%=16%;答:所得溶液中溶质的质量分数是16%.
分析:由于氧化钠能够和水发生化学反应,因此所得溶液中的溶质是生成的氢氧化钠,由于在反应的过程中并没有沉淀和气体生成,因此溶液的质量则为氧化钠和水的质量总和;最后根据溶质质量分数=
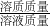 ×100%即可求得所得溶液中溶质的质量分数.
×100%即可求得所得溶液中溶质的质量分数.点评:本题难度较大,主要考查了有关化学方程式的溶液中溶质的质量分数的计算,培养学生的综合应用能力;关键是要知道溶液的溶质是谁.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目