题目内容
2. 请根据如图所示的实验过程和提供的数据(杂质不溶于水,也不与稀盐酸反应.产生的气体全部逸出),回答下列问题:
请根据如图所示的实验过程和提供的数据(杂质不溶于水,也不与稀盐酸反应.产生的气体全部逸出),回答下列问题:(1)生成二氧化碳氢气的质量为4.4g.
(2)大理石中碳酸钙的质量分数(精确到0.1%,写出计算过程).
分析 根据图中信息可以知道,反应前加入的物质的总质量为:15g+100g,而反应后烧杯内物质的总质量为110.6g,根据质量守恒定律可知道物质减少的质量为生成二氧化碳的质量,据此由反应的化学方程式可计算出碳酸钙的质量.
解答 解:
(1)根据图中信息可以知道,反应前加入的物质的总质量为:15g+100g,而反应后烧杯内物质的总质量为110.6g,根据质量守恒定律可知道物质减少的质量为生成二氧化碳的质量,反应中生成CO2的质量为:15g+100g-110.6g=4.4g
(2)设15g大理石中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10g
大理石中碳酸钙的质量分数=$\frac{10g}{15g}×$100%≈66.7%.
答:
(1)4.4g;
(2)大理石中碳酸钙的质量分数为66.7%
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意(或图表信息)等各种信息,根据质量守恒定律计算出二氧化碳气体的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.现有稀硫酸、烧碱溶液、氯化钡溶液、硫酸铜溶液、二氧化碳气体六种物质两两混合后共能发生多少个反应( )
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
10.如图所示装置气密性良好,试管中装有稀盐酸.向试管中加入某物质后,温度计温度升高,该物质是( )

| A. | 镁条 | B. | 碳酸钙 | C. | 硝酸铵 | D. | 氯化钠 |
7.下列对宏观现象的微观解释错误的是( )
| A. | 50mL酒精和50mL水混合后体积小于100mL,是因为分子之间存在间隔 | |
| B. | 太阳光照射下,湿衣服上的水干得更快是因为温度高分子运动加快 | |
| C. | 缉毒犬能根据气味发现毒品,是因为分子在不断地运动 | |
| D. | 温度计受热时水银柱上升,是因为汞原子受热时体积变大 |
 ”“
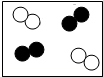
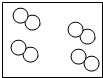
”“ ”分别表示两种不同质子数的原子其中表示化合物的是( )
”分别表示两种不同质子数的原子其中表示化合物的是( )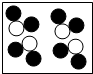

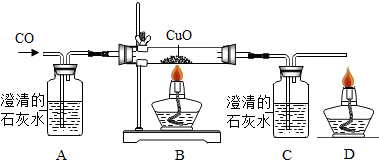 甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.