题目内容
14.将一定质量的a,b,c,d四种物质放入一密闭容器中,一定条件下反应一段时间后,测得反应前后各物质如下表所示,下列说法中正确的是( )| 物质 | a | b | c | d |
| 反应前的质量(g) | 10 | 10 | 10 | 2 |
| 反应后的质量(g) | X | 2 | 21 | 2 |
| A. | b是生成物 | B. | X的值为7 | ||
| C. | 参加反应的b,c,质量比为2:21 | D. | d一定是该反应的催化剂 |
分析 根据化学反应前后质量减少的是反应物,质量增加的是生成物,由表格的数据结合质量守恒定律可以完成反应物和生成物的判断,进而结合基本反应类型的特点来完成解答即可.
解答 解:A、反应后b的质量减少,是反应物,说法错误;
B、根据质量守恒定律反应后a物质的质量是:(10g+10g+10g+2g)-(2g+21g+2g)=7g,说法正确;
C、参加反应的bc质量比为(10-2)g:(21-10)g=8:11,说法错误:
D、d物质的质量反应前后质量不变,可能是该反应的催化剂,也可能不参加反应,说法错误;
故选B.
点评 此题是结合质量守恒定律和化合反应的特征来判断反应类型,解此题的关键是要会正确分析判断那些物质是反应物,那些物质是生成物.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下表是生活中一些物质的PH
有关它的说法正确的是( )
| 物质种类 | 厕所清洁剂 | 橘子汁 | 牛奶 | 草木灰水 | 厨房清洁剂 |
| PH | 1 | 3 | 6.5 | 11 | 12.5 |
| A. | 草木灰可改良碱性土壤 | B. | 橘子汁能使酚酞试液变红 | ||
| C. | 牛奶酸性比橘子强 | D. | 胃酸过多的人不易多吃橘子 |
5.某同学在医院输液时,发现医生给他输的是溶质质量分数为0.9%的生理盐水.若他想要回家自制500g的生理盐水,则他应该称量的食盐质量为( )
| A. | 0.45g | B. | 4.5g | C. | 45g | D. | 450g |
9.下列灭火方法不合理的是( )
| A. | 炒菜时油锅不慎着火,可用水扑灭 | |
| B. | 森林发生火灾,可砍掉部分树木,形成隔离带 | |
| C. | 堆放杂物的纸箱着火,用水浇灭 | |
| D. | 不慎碰到酒精灯,酒精在桌面上燃烧,立即用湿抹布扑盖 |
19.对比分析是化学研究和学校的基本方法,为了验证化学反应是否遵守质量守恒定律,甲、乙、冰三个兴趣小组的同学分别设计了如图所示的实验.
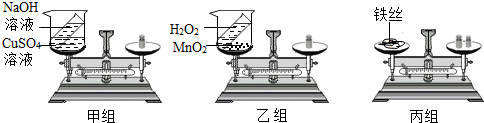
【实验步骤】如图所示,甲、乙两组同学分别把盛有适量NaOH、H2O2溶液的小试管放入盛有CuSO4溶液、MnO2溶液的烧杯中,并将烧杯放到天平上调至平衡,接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡,丙组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上,用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却后将所得的物质与石棉网一起再放回托盘天平上称量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
(2)通过对上述实验的对比分析,甲丙两组同学发现乙同学的结论是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致乙组实验实验反应后天平不平衡的原因是反应生成的氧气逸散到空气中,质量减少.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】从微观角度分析化学反应遵守质量守恒定律的原因是:化学反应前后,原子的质量、种类、数目均不变.

【实验步骤】如图所示,甲、乙两组同学分别把盛有适量NaOH、H2O2溶液的小试管放入盛有CuSO4溶液、MnO2溶液的烧杯中,并将烧杯放到天平上调至平衡,接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡,丙组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上,用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却后将所得的物质与石棉网一起再放回托盘天平上称量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | 化学方程式 | 结论 | |
| 甲组 | 产生蓝色沉淀,天平①平衡(填“平衡”或“不平衡”) | ②2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 | 该反应遵守质量守恒定律 |
| 乙组 | 烧杯中产生大量气泡,天平不平衡 | ③2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | 该反应不遵守质量守恒定律 |
| 丙组 | ④剧烈燃烧,火星四射,生成黑色固体,反应前后称量质量不相等 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | 该实验遵守质量守恒定律 |
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】从微观角度分析化学反应遵守质量守恒定律的原因是:化学反应前后,原子的质量、种类、数目均不变.
6.甲、乙、丙、丁四种物质,它们在密闭容器中反应前后的变化关系如下表所示,则下列说法错误的是( )
| 物质名称 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 8 | 32 | 5 | 4 |
| 反应后质量/g | 16 | 4 | x | 24 |
| A. | 该反应为分解反应 | |
| B. | 丙可能是该反应的催化剂 | |
| C. | 该反应中参与反应的甲、乙两物质的质量比为1:4 | |
| D. | 乙中含有两种或两种以上的元素 |
3.除去括号内杂质的方法正确的是( )
| A. | N2(O2):放入过量木炭充分燃烧 | B. | CO2(CO):通入足量石灰水中 | ||
| C. | Fe(Zn):加入足量稀盐酸 | D. | MnO2(KCl):溶解、过滤、洗涤、干燥 |
4.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 铁丝在氧气中燃烧 2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 化合反应 | |
| B. | 比较铜和银的活动性 Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| C. | 用稀硫酸除铁锈 Fe2O3+2H2SO4═2FeSO4+3H2O 复分解反应 | |
| D. | 除去氧化钙中的碳酸钙 CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ 分解反应 |
